<<Մետաղների քիմիական հատկությունները>>



Բույսերն իրենց անհրաժեշտ տարրերը կլանում են հողից, իոնների ձևով՝/NH4/+, /NO3/—,K+ , /H2PO4/—,Fe3+ , Cu2+ և այլն: Երեք կարևոր տարր՝ ազոտը, ֆոսֆորը և կալիումը, անհրաժեշտ են բույսերին մեծ քանակություններով, ուստիև այդ տարրերը պարունակող տարրերը պարունակող պարարտանյութերն ստանում են արդյունաբերական մասշտաբներով:
Կենսական տարրերն այն քիմիական տարրի ատոմներն են, որոնք առաջացնում են այն նյութերը, որոնք ապահովում են կենդանի օրգանիզմների կենսագործունեությունը:
Մակրո տարրեր.
Ածխածին/C/ , ջրածին/H/, թթվածին/O/, ազոտ/N/, ֆոսֆոր/P/, ծծումբ/Si/:
Միկրո տարրեր.
Կալցիում/Ca/, մագնեզիում/Mg/, երկաթ/Fe/, կալիում/K/, նատրիում/Na/, ցինկ/Zn/, կոբալտ/Co/, պղինձ/Cu/, ֆտոր/F/, քլոր/Cl/, բրոմ/Br/, յոդ/I/:
կարմիր գույնով նշել եմ թեմաները, իսկ կապույտ գույնով նշել եմ հարցերը իսկ պատասխանները մգացրել եմ.
Բույսերի վնասատուների դեմ պայքարի և կենսաբանական փոշոտման միջոցներ: Այս միջոցները հնարավորություն են տալիս էկոլոգիապես մաքուր եղանակներով ապահովել բարձր բերքատվություն, ինչի շնորհիվ լայն կիրառություն են ստացել ամբողջ աշխարհում: Բույսերի կենսաբանական փոշոտման և վնասատուների դեմ պայքարի միջոցներն արդեն հաջողությամբ կիրառվում են Հայաստանում` բուսաբուծական արտադրության բոլոր ոլորտներում` այգիներ, տնկարաններ, դաշտեր, և հատկապես հիանալի արդյունք են ապահովում ծաղիկների, հատապտուղների և բանջարեղենի ջերմատներում ու ջերմոցներում: Յուրաքանչյուրառաջադրանքը 0.5միավոր է
Փորձերի համար անհրաժեշտ են նատրիում, կալցիում, մագնեզիում, ցինկ, երկաթ, աղաթթու,
հայտանյութ ֆենոլֆտալեին, պղնձարջասպի լուծույթ:
Լաբորատոր փորձ 1. <<Հրավառություն>>՝ մագնեզիումի ժապավենի այրումը:Գրեք ընթացող ռեակցիայի հավասարումը:
Mg+O2 =2MgO+Q
Լաբորատոր փորձ 2. Ակտիվ մետաղներից նատրիումի կամ կալցիումի փոխազդեցությունը
ջրի հետ:Համոզվելու համար, որ առաջացել է ալկալի` կաթոցիկով 2
կաթիլ հայտանյութ ֆենոլֆտալեին լցրեք առաջացած ալակալու
լուծույթին : Գրեք ընթացող ռեակցիայի հավասարումը:
2Na+2H2O
Լաբորատոր փորձ 3. Միջին ակտիվության մետաղներից` մագնեզիումի, ցինկի, ալյումինի
փոխազդեցությունը նոսր ծծմբական թթվի կամ աղաթթվի հետ
անջատվող ջրածնի այրումը: Գրեք համապատասխան ռեակցիաների
հավասարումները:
Zn+2HCl=ZnCl2+H2
Mg+2HCl —>MgCl2+H2
Լաբորատոր փորձ 4. Մետաղի փոխազդեցությունը աղերի ջրային լուծույթների հետ(բացի
ալկալիական և հողալկալիական մետաղների, ինչու՞): Երկաթի(մեխի)
փոխազդեցությունը պղնձարջասպի լուծույթի հետ: Ինչու՞ է մեխը
կարմրում: Գրեք ընթացող ռեակցիայի հավասարումը: - Մետաղների ընդհանուր բնութագրումը, ատոմների կառուցվածքը
Ըստ Մենդելեևի Պարբերական աղյուսակի քիմիական տարրերը բաժանվում են.- Մետաղների
- Ոչ մետաղների
- Մետաղանմաններ
Մետաղները կազմում են այդ տարրերի 76.2%-ը։
Պարզ մետաղ կոչվում է հիմնականում մետաղական մեկ տարրից բաղկացած նյութը։ Մետաղները ոչ մետաղներից և կիսահաղորդիչներից տարբերող բնորոշ հատկանիշներն են՝ ջերմաստիճանի իջեցմանը համեմատ աճող բարձր էլեկտրահաղորդականությունը, պլաստիկությունը, լույս անդրադարձնելու ունակությունը(մետաղական փայլ), և բարձր ջերմահաղորդականությունը։ Այս հատկությունները պայմանավորված են մետաղական տարրերի ատոմների կառուցվածքի առանձնահատկությամբ։
Ցանկացած մետաղական տարրի ատոմ կազմված է դրական լիցքավորված միջուկից (պրոտոններից և նեյտրոններից) և նրա շուրջը արագ պտտվող բացասական լիցքավորված էլեկտրոններից։ Պրոտոնի և էլեկտրոնի լիցքերը մեծությամբ հավասար են, նշաններով հակադիր, իսկ ատոմում նրանց թիվը հավասար։ Ատոմի արտաքին թաղանթում կարող են գտնվել 1-8 վալենտային էլեկտրոններ։ Մետաղական տարրերի ատոմները ունեն նվազագույն թվով վալենտային էլեկտրոններ՝ առավելապես 1 և 2, հազվադեպ՝ 3։ Թույլ վալենտային էլեկտրոնները պոկվում են ատոմից՝ մետաղի հեղուկ կամ պինդ վիճակում, և նորից միանում նրանցից որևէ մեկին։ Որքան մեծ է ազատ էլեկտրոնների կոնցենտրացիան, այնքան խիստ են արտահայտված տարրի մետաղական հատկությունները։ Ազատ էլեկտրոնների այդ ամբողջությունը կոչում են էլեկտրոնային գազ։ Մետաղների դրական լիցքավորված իոնների և բացասական լիցքավորված էլեկտրոնային գազի միջև էլեկտրական ձգման ուժերը ամուր կապ են ստեղծում մետաղի ատոմների միջև, որը կոչվում է մետաղական կապ։
Մետաղների ատոմային կառուցվածքը յուրահատուկ է, այդ իսկ պատճառով նրանք օժտված են բազմաթիվ հատկություններով, և ամենալայն կիրառությունը ունեն մինչ այժմ, հիմա և հետագայում։
Ցանկացած մետաղական տարրի ատոմ կազմված է դրական լիցքավորված միջուկից (պրոտոններից և նեյտրոններից) և նրա շուրջը արագ պտտվող բացասական լիցքավորված էլեկտրոններից։ Պրոտոնի և էլեկտրոնի լիցքերը մեծությամբ հավասար են, նշաններով հակադիր, իսկ ատոմում նրանց թիվը հավասար։ Ատոմի արտաքին թաղանթում կարող են գտնվել 1-8 վալենտային էլեկտրոններ։ Մետաղական տարրերի ատոմները ունեն նվազագույն թվով վալենտային էլեկտրոններ՝ առավելապես 1 և 2, հազվադեպ՝ 3։ Թույլ վալենտային էլեկտրոնները պոկվում են ատոմից՝ մետաղի հեղուկ կամ պինդ վիճակում, և նորից միանում նրանցից որևէ մեկին։ Որքան մեծ է ազատ էլեկտրոնների կոնցենտրացիան, այնքան խիստ են արտահայտված տարրի մետաղական հատկությունները։ Ազատ էլեկտրոնների այդ ամբողջությունը կոչում են էլեկտրոնային գազ։ Մետաղների դրական լիցքավորված իոնների և բացասական լիցքավորված էլեկտրոնային գազի միջև էլեկտրական ձգման ուժերը ամուր կապ են ստեղծում մետաղի ատոմների միջև, որը կոչվում է մետաղական կապ։
Մետաղների ատոմային կառուցվածքը յուրահատուկ է, այդ իսկ պատճառով նրանք օժտված են բազմաթիվ հատկություններով, և ամենալայն կիրառությունը ունեն մինչ այժմ, հիմա և հետագայում։
- Մետաղների դիրքը քիմիական տարրերի պարբերական համակարգում
Պարբերական համակարգում մետաղները մոտավորապես չորս անգամ շատ են ոչ մետաղներից.
Յուրաքանչյուր պարբերություն սկսվում է ակտիվ մետաղով/ալկալիական մետաղ/ և ավարտվում է ոչ մետաղներով:
Մետաղների շատությունը պայմանավորված է շառավիղների համեմատական մեծությամբ: - Մետաղական քիմիական կապը
Մետաղական կապ
Մետաղային տարրերի ատոմներն արտաքին էներգիական մակարդակում ունեն քիչ թվով էլեկտրոններ, հիմնականում՝ 1 կամ 2, առավել քիչ դեպքերում՝ 3 և 4 էլեկտրոններ։ Ոչմետաղների համեմատ, մետաղներն ունեն մեծ ատոմային շառավիղ, որի պատճառով վալենտային էլեկտրոնները թույլ են ձգվում միջուկների կողմից։ Անգամ քիչ էներգիայի առկայությամբ էլեկտրոնները կարող են անցնել ավելի բարձր էներգիական մակարդակներ կամ նույնիսկ հեռանալ ատոմից։ Բյուրեղային վիճակում մետաղների ատոմներն իրար կողքի լինելիս վալենտային էլեկտրոնները, ինչպես կովալենտային կապի ժամանակ, ընդհանրացվում են։ Սակայն, ի տարբերություն կովալենտային կապի, այդ ընդհանրացումը կատարվում է ոչ թե երկու ատոմների, այլ մետաղի բյուրեղում եղած բոլոր ատոմների միջև։ Oրբիտալներն ընդհանրացվելով առաջացնում են մի վիթխարի «գերօրբիտալ»՝ բացասականապես լիցքավորված «էլեկտրոնային գազ», որով կարծես ամրացվում են մետաղի դրական իոնները։ Մետաղային կապը ապատեղայնացված կապ է, գործում է ոչ թե երկու կամ իր շուրջը գտնվող մի քանի ատոմների, այլ մետաղի կտորի բոլոր ատոմների միջև։ Մետաղային կապին բնորոշ է մետաղական բյուրեղացանցը, որի հանգույցներում մետաղի դրական իոններն են՝ շրջապատված ազատորեն տեղաշարժվող վալենտային էլեկտրոններով։ Մետաղային կապին և մետաղային բյուրեղացանցին բնորոշ են պլաստիկությունը, լավ էլեկտրա– և ջերմահաղորդականությունը, մետաղական փայլը։ ՄԵՏԱՂՆԵՐ Մետաղների ֆիզիկական հատկությունները
Մետաղների ֆիզիկական հատկություններ
Բարիում

Ալյումին

Բոլոր մետաղները (բացի սնդիկից և պայմանականորեն ֆրանսիումից) սովորական պայմաններումգտնվում են պինդ ագրեգատային վիճակում, սակայն ունեն տարբեր կարծրություն: Ստորև ներկայացված են մի շարք մետաղների կարծրությունները՝ ըստ Մոոսի շարքի.
Մաքուր մետաղների հալման ջերմաստիճանը տատանվում է -39оС-ից (սնդիկ) 3410о С միջակայքում (Վոլֆրամ)։ Մետաղների մեծամասնության հալման ջերմաստիճանը (ալկալիական մետաղներից բացի) բարձր է, սակայն որոշ «նորմալ» մետաղները, ինչպիսիք են օրինակ անագն ու կապարը, կարելի է հալեցնել հասարակ էլեկտրական կամ գազային վառարանի վրա։
Կախված խտությունից՝ մետաղները լինում են թեթև (խտությունը 0,53 ÷ 5 գ/սմ3) և ծանր (5 ÷ 22,5 գ/սմ³)։ Ամենաթեթև մետաղն է լիթիումը ( խտությունը 0.53 գ/սմ³)։ Ամենածանր մետաղը ներկա պահին անվանել հնարավոր չէ, քանի որ ամենածանր մետաղների՝ օսմիումի և իրիդիումի, խտությունները գրեթե հավասար են (մոտ 22.6 գ/սմ³ — ճիշտ 2 անգամ ավելի, քան կապարի խտությունն է), իսկ դրանց ստույգ խտության հաշվումը չափազանց դժվար է՝ դրա համար անհրաժեշտ է լրիվ մաքրել մետաղը, քանի որ յուրաքանչյուր խառնուրդ ցածրացնում է դրանց խտությունը։
Մետաղների մեծամասնությունը պլաստիկ է, այսինքն մետաղյա լարը կարելի է թեքել, և այն չի կոտրվի։ Սա տեղի է ունենում մետաղների ատոմների շերտերի՝ առանց նրանց միջև կապի խախտման տեղաշարժերի պատճառով։ Ամենապլաստիկ մետաղներն են ոսկին, երկաթն ու պղինձը: Ոսկուց կարելի է պատրաստել 0.003 մմ հաստությամբ թիթեղ, որը կիրառվում է իրեղենի ոսկեպատման համար։ Սակայն ոչ բոլոր մետաղներն են պլաստիկ։ Ցինկի և անագի լարը ճռթճռթում է՝ այն թեքելիս, մանգանն ու բիսմութը, դեֆորմացիայի ենթարկվելիս, գրեթե ընդհանրապես չեն թեքվում, այլ միանգամից կոտրվում են։
Պլաստիկությունը կախված է նաև մետաղի մաքրությունից. այդպես՝ շատ մաքուր քրոմը բավականին պլաստիկ է, սակայն դրանում չնչին խառնուրդի դեպքում, այն դառնում է փխրուն և ավելի կարծր։ Որոշ մետաղներ, ինչպիսիք են ոսկին, արծաթը, կապարը, ալյումինը, օսմիումը, կարող են միաձուլվել իրար հետ, սակայն դա կխլի տասնյակ տարիներ։
Բոլոր մետաղները էլեկտրական հոսանքի լավ հաղորդիչներ են, սա պայմանավորված է դրանց բյուրեղային ցանցում առկա շարժուն էլեկտրոններով, որոնք շարժվում են էլեկտրական դաշտի ազդեցության տակ։ Արծաթը, պղինձն ու ալյումինը ունեն ամենաբարձր էլեկտրահաղորդականությունը, որի պատճառով վերջին երկուսը հաճախակի օգտագործվում են հաղորդալարերի պատրաստման համար։ Բարձր էլեկտրահաղորդականություն ունի նաև նատրիումը: Փորձարարական տեխնիկայում հայտնի են նատրիումային էլեկտրահաղորդալարերի՝ նատրիումով լցված չժանգոտվող պողպատից խողովակների, կիրառման փորձեր։ Նատրիումի ցածր տեսակարար զանգվածի շնորհիվ, հավասարաչափ դիմադրության դեպքում նատրիումային լարերը ստացվում են պղնձյա և նույնիսկ ալյումինե լարերից զգալիորեն թեթև։
Մետաղների բարձր ջերմահաղորդականությունը նույնպես կախված է ազատ էլեկտրոնների շարժունակությունից։ Այդ պատճառով ջերմահաղորդականության շարքը նման է էլեկտրահաղորդականության շարքին, ուստի ջերմության, ինչպես նաև էլեկտրական հոսանքի ամենալավ հաղորդիչը հանդիսանում է արծաթը: Նատրիումը նույնպես կիրառվում է, որպես ջերմության լավ հաղորդիչ։ Լայն տարածված է նատրիումի օգտագործումը օրինակ ավտոմոբիլային շարժիչների կափույրների սառեցման և բարելավման համար։
Մետաղների մեծամասնության գույնը գրեթե նունն է՝ բաց մոխրագույն՝ երկնագույն երանգով։ Ոսկին, պղինձն ու ցեզիումը համապատասխանաբար դեղին, կարմիր և բաց դեղին գույնի են։
- Մետաղների քիմիական հատկությունները՝ փոխազդեցությունը պարզ և բարդ նյութերի հետ
Մետաղների քիմիական հատկություններ

Լիթիումի քլորիդ
Մետաղների մեծամասնության արտաքին էներգիական մակարդակում առկա է էլեկտրոնների փոքր քանակ (1-3), այդ պատճառով նրանք ռեակցիաների մեծ մասում հանդես են գալիս որպես վերականգնողներ (այսինքն «տալիս են» իրենց էլեկտրոնները)։
Պարզ նյութերի հետ փոխազդեցությունը
- Թթվածնի հետ փոխազդում են բոլոր մետաղները, բացի ոսկուց և պլատինից: Արծաթի հետ փոխազդեցությունը նկատվում է միայն բարձր ջերմաստիճանների դեպքում, սակայն արծաթի (II) օքսիդը գրեթե չի առաջանում, քանի որ այն ջերմապես անկայուն է։ Կախված մետաղի տեսակից՝ ելանյութը կարող է լինել օքսիդ, պերօքսիդ:
{ {4Li+O_{2}=2Li_{2}O} } լիթիումի օքսիդ
{{2Na+O_{2}=Na_{2}O_{2}} } նատրիումի պերօքսիդ
{ {K+O_{2}=KO_{2}} } կալիումի գերրօքսիդ
Պերօքսիդից օքսիդ ստանալու համար պերօքսիդը վերականգնվում է մետաղի միջոցով.
{{Na_{2}O_{2}+2Na=2Na_{2}O} }
Միջին և ցածր ակտիվության մետաղների հետ ռեակցիան անցնում է տաքացման միջոցով.
{{3Fe+2O_{2}=Fe_{3}O_{4}} }
{{2Hg+O_{2}=2HgO} }
{{2Cu+O_{2}=2CuO} }
{{2Na+O_{2}=Na_{2}O_{2}} } նատրիումի պերօքսիդ
{ {K+O_{2}=KO_{2}} } կալիումի գերրօքսիդ
Պերօքսիդից օքսիդ ստանալու համար պերօքսիդը վերականգնվում է մետաղի միջոցով.
{{Na_{2}O_{2}+2Na=2Na_{2}O} }
Միջին և ցածր ակտիվության մետաղների հետ ռեակցիան անցնում է տաքացման միջոցով.
{{3Fe+2O_{2}=Fe_{3}O_{4}} }
{{2Hg+O_{2}=2HgO} }
{{2Cu+O_{2}=2CuO} }
- Ազոտի հետ փոխազդում են միայն ամենաակտիվ մետաղները, սենյակային ջերմաստիճանում փոխազդում է միայն լիթիումը՝ կազմելով նիտրիդներ:
{{6Li+N_{2}=2Li_{3}N} }
Տաքացման ժամանակ՝
{{2Al+N_{2}=2AlN} }
{ {3Ca+N_{2}=Ca_{3}N_{2}} }
Տաքացման ժամանակ՝
{{2Al+N_{2}=2AlN} }
{ {3Ca+N_{2}=Ca_{3}N_{2}} }
- Ծծմբի հետ փոխազդում են բոլոր մետաղները՝ բացի ոսկուց ու պլատինից.
Երկաթը փոխազդում է ծծմբի հետ տաքացման դեպքում, կազմելով սուլֆիդ:
{ {Fe+S=FeS} }
{ {Fe+S=FeS} }
- Ջրածնի հետ փոխազդում են միայն ամենաակտիվ մետաղները, այսինքն IA և IIA խմերի տարրերը, բացառությամբ բերիլիումի: Ռեակցիաները իրականացվում են տաքացման դեպքում՝ կազմելով հիդրիդներ: Ռեակցիաներում մետաղը հանդիսանում է վերականգնող, ջրածնի օքսիդացման աստիճանը -1 է։
{ {2Na+H_{2}=2NaH} }
{ {Mg+H_{2}=MgH_{2}} }
{ {Mg+H_{2}=MgH_{2}} }
- Ածխածնի հետ փոխազդում են միայն ամենաակտիվ մետաղները, ընդ որում՝ ռեակցիայի ընթացքում ստացվում են ացետիլենիդներ կամ մեթանիդներ: Ացետիլենիդները ջրի հետ փոխազդելիս տալիս են աթետիլեն, մեթանիդները՝ մեթան:
{{2Na+2C=Na_{2}C_{2}} }
{{Na_{2}C_{2}+2H_{2}O=2NaOH+C_{2}H_{2}} }
{{Na_{2}C_{2}+2H_{2}O=2NaOH+C_{2}H_{2}} }
- Մետաղների ստացման եղանակները`լաբորատորիայում և արդյունաբերական
Մետալուրգիա, սկզբնական նեղ իմաստով՝ հանքաքարից մետաղների արտազատման արվեստ։ Արդի նշանակությամբ՝ գիտության ու տեխնիկայի բնագավառ և արդյունաբերության ճյուղ, որոնք ընդգրկում են հանքաքարից կամ այլ նյութերից մետաղների ստացման, ինչպես նաև դրանց քիմիական բաղադրության, կառուցվածքի և մետաղական համաձուլվածքների հատկությունների փոփոխման հետ կապված պրոցեսներ։ Մետալուրգիային են վերաբերում նաև երկրի ընդերքից ստացված մետաղների ու համաձուլվածքների նախնական մշակման ու դրանց ձևի և հատկությունների փոփոխման պրոցեսները (զտում, ձուլում, ճնշմամբ մշակում, ջերմամշակում և այլն)։ - Մետաղների կիրառման բնագավառները:
Մետաղամշակումը լայն կիռարում ուներ նաև զենքի և զինամթերքի արտադրության ասպարեզում։ Հարձակողական և պաշտպանական զենքը կազմված էր տարբեր ձևերի նիզակներից, դաշույններից, թրերից, կացիններից, գուրզերից։ Գտնվել են նաև ոսկուց և արծաթից օրինակներ։
Մետալուրգիան Հայաստանում
ՀԽՍՀ-ում զգալի զարգացում ստացավ պղնձի մետալուրգիան (Ալավերդու լեռնամետալուրգիական կոմբինատ), ալյումինի մետալուրգիան (Քանաքեռի ալյումինի գործարան), պղնձամոլիբդենային և բազմամետաղ հանքաքարերի հարստացման արտադրությունը (Զանգեզուրի պղնձամոլիբդենային կոմբինատ)։ Կիրառում գտան նաև պղնձի փոշեմետալուրգիան և երկաթի ուղղակի վերականգնման պրոցեսները։ Ժամանակակից մետալուրգիական արտադրության համար բնորոշ են՝ հումքի լրիվ օգտագործումը, բազմամետաղ հանքաքարերի կոմպլեքսային մշակումը, արտադրության կազմակերպումն առանց թափոնների, արտադրական պրոցեսների մեքենայացման ու ավտոմատացման բարձր մակարդակը։ Կենսական տարրեր
Բույսերի բնականոն աճի ու զարգացման համար մոտ 22 քիմիական տարր է անհրաժեշտ: Առանձնապես կարևոր է կալիում/K/, ազոտ/N/, ֆոսֆոր/P/, ածխածին/C/, թթվածին/O/ և ջրածին/H/ տարրերի նշանկությունը: Պակաս քանակություններով, բայց՝ պարտադիր, պահանջվում են կալցիում, մագնեզիում, երկաթ և այլ տարրեր: Իսկ որոշ տարրեր /պղինձ, կոբալտ, ցինկ և այլն/ չնչին քանակություններով են անհրաժեշտ, սակայն հողում այդ տարրերի իսպառ բացակայությունը բույսերի համար կործանարար է:Բույսերն իրենց անհրաժեշտ տարրերը կլանում են հողից, իոնների ձևով՝/NH4/+, /NO3/—,K+ , /H2PO4/—,Fe3+ , Cu2+ և այլն: Երեք կարևոր տարր՝ ազոտը, ֆոսֆորը և կալիումը, անհրաժեշտ են բույսերին մեծ քանակություններով, ուստիև այդ տարրերը պարունակող տարրերը պարունակող պարարտանյութերն ստանում են արդյունաբերական մասշտաբներով:
Կենսական տարրերն այն քիմիական տարրի ատոմներն են, որոնք առաջացնում են այն նյութերը, որոնք ապահովում են կենդանի օրգանիզմների կենսագործունեությունը:
Մակրո տարրեր.
Ածխածին/C/ , ջրածին/H/, թթվածին/O/, ազոտ/N/, ֆոսֆոր/P/, ծծումբ/Si/:
Միկրո տարրեր.
Կալցիում/Ca/, մագնեզիում/Mg/, երկաթ/Fe/, կալիում/K/, նատրիում/Na/, ցինկ/Zn/, կոբալտ/Co/, պղինձ/Cu/, ֆտոր/F/, քլոր/Cl/, բրոմ/Br/, յոդ/I/:
- Մարդկությանը հուզող ինչպիսի՞ էկոլոգիական հիմնախնդիրներ գիտեք:
1. Երկրագնդի մթնոլորտի աղտոտումը և օզոնի շերտի քայքայում:
2. Երկրագնդի անտառահատումը:
3. Անապատացումը:
4. Համաշխարհային օվկիանոսի աղտոտումը:
5. Քաղցրահամ ջրերի որակի վատացումը:
- Ո՞րն է էկոլոգիապես մաքուր սնունդը:
Էկոլոգիապես մաքուր սնունդն այն է, երբ վերջնական արտադրանք ստանալու ամբողջ ընթացքում պահպանվում են էկոլոգիական բոլոր նորմերը: Էկոլոգիապես մաքուր սնունդը չի պարունակում իր մեջ այնպիսի վնասակար նյութեր, որոնք թողնում են բացասական ազդեցություն մարդու առողջության վրա:
- Ի՞նչ կարծիք ունեք կենսական միջավայրի մասին:
- Որո՞նք են առողջ ապրելակերպի սկզբունքները:
Որոառողջ ապրելակերպի սկզբունքները ըստ Ճապոնացի գիտնականների`
- Էկոլոգիապես մաքուր սնունդ, մաքուր խմելու ջուր, մոքուր օդ:
- Առողջ քուն` 8 ժամ (քնել ժամը 22:00-23:00)
- Մարմնակրթություն, հիգենա
- Առաջին երրեք կետերի կատարում, վատ սովորություն ներից ձեռբազատում:
- ՍՏՐԵՍԱՅԻՆ իրավիճակներից դուրս գալ կատակով, հումորով և ծիծաղով:
- Ո՞րն է համարվում մաքուր խմելու ջուր:
- Ջրի շրջապտույտը բնության մեջ:
Ջուրն անընդհատ «կռվի» մեջ է քարոլորտի հետ: Հոսող ջրերը պոկում են ժայռաբեկորներ, քշում-տանում բերրի հողը, ջարդում-մանրացնում ապարները, քանդում ափերն ու հունը, փորում անդնդախոր կիրճեր, հարթավայրերում կուտակում նստվածքներ և այլն:
- Ջրի աղտոտման տեսակները որո՞նք են:
Ջրի աղտոտման հիմնական աղբյուրներն են արդյունաբերական և կենցաղային հոսքաջրերը, ձնհալի և անձրևների ժամանակ հողահանդակներից տեղափոխված պեստիցիդները բնակավայրերից վնասակար նյութերը, անձրևի և ձյան միջոցով՝ մթնոլորտից անջատվող աղտոտող նյութերը։
- Ի՞նչ է կոշտ ջուրը և ինչպե՞ս են այն վերացնում:
Կոշտ ջրում առկա է մագնեզիումի, կալցիումի լուծելի աղե:
- Բույսերի պաշտպանություն` բույսերի, բուսական արտադրանքի աճեցման, փորձարկման, պահպանման և փոխադրման վայրերում վնասակար օրգանիզմների դեմ քիմիական և կենսաբանական պայքարի միջոցների օգտագործում:
- Ի՞նչ են ագրոքիմիկատները` Ագրոքիմիկատները պարարտանյութերը, քիմիական հողաբարելավիչները, որոնք նախատեսված են բույսերի սնուցման, հողերի բերրիության բարելավման համար:
- Ի՞նչ է պեստիցիդը` Պեստիդը բույսերի պաշտպանության միջոց է, ցանկացած նյութ կամ նյութերի խառնուրդ, որը նախատեսված է որոշակի վնասատուների (ներառյալ մարդկանց և կենդանիների հիվանդություններ փոխանցողների, սննդամթերքի, գյուղատնտեսական արտադրանքի, փայտանյութի, կենդանիների կերերի արտադրության, վերամշակման, փոխադրման, իրացման գործընթացներին խանգարող և խոչընդոտող վնասատուների), բույսերի և սնկերի անցանկալի տեսակների կանխարգելման, ոչնչացման կամ պայքարի համար: Պեստիցիդների խմբում ներառված են միջատասպանները (ինսեկտիցիդներ), կրծողների դեմ պայքարի միջոցները (ռոտենդիցիդներ)։
- Ի՞նչ է սնկասպանները` Սնկասպանները (ֆունգիցիդներ), մոլախոտերի դեմ պայքարի համար նախատեսված նյութերը (հերբիցիդներ), բույսերի աճի կարգավորիչները, ֆերոմոնները, դեֆոլիանտները, դեսիկանտները և ֆումիգանտները։
Որո՞ նք են բույսերի պաշտպանության միջոցները՝
Բույսերի պաշտպանության միջոցներն են`
- բույսերի վնասակար օրգանիզմների կանխարգելում
- դրանց դեմ պայքարի և վերացման համար կիրառվող քիմիական և կենսաբանական միջոցներ
- Ո՞րն է համարվում մաքուր խմելու ջուր
Մաքուր խմելու ջուրը պետք է պարունակի հանքային աղեր` դառը անհամ ջուրը: Եթե ջուրը բաղկացած է 100մանրէ
- Ջրի շրջապտույտը բնության մեջ
- Ջրի աղտոտման տեսակները որո՞նք են
- Ի՞նչ է կոշտ ջուրը և ինչպե՞ս են այն վերացնում
Անհատական-հետազոտական աշխատանքների թեմաները.
- Մթնոլորտի աղտոտումը, թունավոր նյութերը օդում:Օդի աղտոտման աղբյուրները:
- Ո՞րն է համարվում մաքուր խմելու ջուր: Ջրի աղտոտման տեսակները:
- Հողի աղտոտումը պեստիցիդների, ագրոքիմիկատների և կենսապատրաստուկների վնասակար մնացորդներով: Բովանդակությունը. Սովորողները կատարելու են լաբորատոր աշխատանքներ գործնական էկոլոգիայից համապատասխան մեթոդական ցուցումներով: Հետազոտելու են տարբեր բնական ջրավազանների ջրի որակի ֆիզիկաքիմիական հատկանիշները` հոտը, գույնը, թթվայնությունը` рН-ը, կատարելու են որակական ռեակցիաներ և որոշելու են սուլֆատների, քլորիդների, ֆոսֆատների և կապարի պարունակությունը մեկ լիտր ջրում և համեմատելու են չափորոշիչների հետ: Նախապատրաստական աշխատանք սովորողների հետ . Սովորողները ինքնուրույն փնտրելու են հետևյալ հարցերի պատասխանները.
- Մարդկությանը հուզող ինչպիսի՞ էկոլոգիական հիմնախնդիրներ գիտեք
- Ո՞րն է էկոլոգիապես մաքուր սնունդը
- Ի՞նչ կարծիք ունեք կենսական միջավայրի մասին
- Որո՞նք են առողջ ապրելակերպի սկզբունքները
- Ո՞րն է համարվում մաքուր խմելու ջուր
- Ջրի շրջապտույտը բնության մեջ
- Ջրի աղտոտման տեսակները որո՞նք են
- Ի՞նչ է կոշտ ջուրը և ինչպե՞ս են այն վերացնում
- Բույսերի պաշտպանություն` բույսերի, բուսական արտադրանքի աճեցման, փորձարկման, պահպանման և փոխադրման վայրերում վնասակար օրգանիզմների դեմ քիմիական և կենսաբանական պայքարի միջոցների օգտագործում:
- Ի՞նչ են ագրոքիմիկատները` պարարտանյութերը, քիմիական հողաբարելավիչները, որոնք նախատեսված են բույսերի սնուցման, հողերի բերրիության բարելավման համար.
- Ի՞նչ է պեստիցիդը` բույսերի պաշտպանության միջոց, ցանկացած նյութ կամ նյութերի խառնուրդ, որը նախատեսված է որոշակի վնասատուների (ներառյալ մարդկանց և կենդանիների հիվանդություններ փոխանցողների, սննդամթերքի, գյուղատնտեսական արտադրանքի, փայտանյութի, կենդանիների կերերի արտադրության, վերամշակման, փոխադրման, իրացման գործընթացներին խանգարող և խոչընդոտող վնասատուների), բույսերի և սնկերի անցանկալի տեսակների կանխարգելման, ոչնչացման կամ պայքարի համար: Պեստիցիդների խմբում ներառված են միջատասպանները (ինսեկտիցիդներ), կրծողների դեմ պայքարի միջոցները (ռոտենդիցիդներ).
- Ի՞նչ է սնկասպանները (ֆունգիցիդներ), մոլախոտերի դեմ պայքարի համար նախատեսված նյութերը (հերբիցիդներ), բույսերի աճի կարգավորիչները, ֆերոմոնները, դեֆոլիանտները, դեսիկանտները և ֆումիգանտները.
- Որո՞ նք են բույսերի պաշտպանության միջոցները՝ բույսերի վնասակար օրգանիզմների կանխարգելման, դրանց դեմ պայքարի և վերացման համար կիրառվող քիմիական, կենսաբանական միջոցներ:
Նախագծի նպատակն է սովորողներին ծանոթացնել հետազոտման գիտական մեթոդներին` դիտարկումներ, փորձեր, փաստեր և կատարել բազմակողմանի վերլուծություններ, նաև կատարել թարգմանություններ`<<Լաբորատոր աշխատանքներ` «Գործնական էկոլոգիայից».
կարմիր գույնով նշել եմ թեմաները, իսկ կապույտ գույնով նշել եմ հարցերը իսկ պատասխանները մգացրել եմ.- Մարդկությանը հուզող ինչպիսի՞ էկոլոգիական հիմնախնդիրներ գիտեք
- Ո՞րն է էկոլոգիապես մաքուր սնունդը
- Ի՞նչ կարծիք ունեք կենսական միջավայրի մասին
- Որո՞նք են առողջ ապրելակերպի սկզբունքները
- Ո՞րն է համարվում մաքուր խմելու ջուր
- Ջրի շրջապտույտը բնության մեջ
- Ջրի աղտոտման տեսակները որո՞նք են
- Ի՞նչ է կոշտ ջուրը և ինչպե՞ս են այն վերացնում
- Բույսերի պաշտպանություն` բույսերի, բուսական արտադրանքի աճեցման, փորձարկման, պահպանման և փոխադրման վայրերում վնասակար օրգանիզմների դեմ քիմիական և կենսաբանական պայքարի միջոցների օգտագործում:
- Ի՞նչ են ագրոքիմիկատները` պարարտանյութերը, քիմիական հողաբարելավիչները, որոնք նախատեսված են բույսերի սնուցման, հողերի բերրիության բարելավման համար.
- Ի՞նչ է պեստիցիդը` բույսերի պաշտպանության միջոց, ցանկացած նյութ կամ նյութերի խառնուրդ, որը նախատեսված է որոշակի վնասատուների (ներառյալ մարդկանց և կենդանիների հիվանդություններ փոխանցողների, սննդամթերքի, գյուղատնտեսական արտադրանքի, փայտանյութի, կենդանիների կերերի արտադրության, վերամշակման, փոխադրման, իրացման գործընթացներին խանգարող և խոչընդոտող վնասատուների), բույսերի և սնկերի անցանկալի տեսակների կանխարգելման, ոչնչացման կամ պայքարի համար: Պեստիցիդների խմբում ներառված են միջատասպանները (ինսեկտիցիդներ), կրծողների դեմ պայքարի միջոցները (ռոտենդիցիդներ).
- Ի՞նչ է սնկասպանները (ֆունգիցիդներ), մոլախոտերի դեմ պայքարի համար նախատեսված նյութերը (հերբիցիդներ), բույսերի աճի կարգավորիչները, ֆերոմոնները, դեֆոլիանտները, դեսիկանտները և ֆումիգանտները.
- Որո՞ նք են բույսերի պաշտպանության միջոցները՝ բույսերի վնասակար օրգանիզմների կանխարգելման, դրանց դեմ պայքարի և վերացման համար կիրառվող քիմիական, կենսաբանական միջոցներ:
Նախագծի նպատակն է սովորողներին ծանոթացնել հետազոտման գիտական մեթոդներին` դիտարկումներ, փորձեր, փաստեր և կատարել բազմակողմանի վերլուծություններ, նաև կատարել թարգմանություններ`<<Լաբորատոր աշխատանքներ` «Գործնական էկոլոգիայից».
Թեմա 1՝ Ենթահարց 1՝ Մթնոլորտի աղտոտում.
Մթնոլորտի աղտոտման հիմնական աղբյուրները
44% Ավտոմեքենա
20% Ջեռուցում
14% Արդյունաբերություն
և 5% Աղբի արյում :
Շրջակա միջավայրի աղտոտումը մարդկանց, բույսերի և կենդանիների կենսագործունեության վրա բացասաբար ազդող նյութերի թույլատրելի քանակի գերազանցումն է միջավայրում: Տարբերում են շրջակա միջավայրի բնածին և մարդահարույց աղտոտիչներ:
Բնածին աղտոտիչներն առաջանում են բնական երևույթների, օրինակ` հրաբուխների, երկրաշարժերի, ջրհեղեղների, հրդեհների պատճառով, իսկ մարդահարույցները՝ մարդու գործունեության հետևանքով: Մարդահարույց աղտոտիչների թվին են դասվում արդյունաբերական, գյուղատնտեսական, տրանսպորտային և կենցաղային թափոնները, էներգիայի տարածումը ջերմության, աղմուկի, ճառագայթման և այլ ձևերով:
Տարբերում են շրջակա միջավայրի աղտոտման 4 ձևեր՝մեխանիկական ,քիմիական, կենսաբանական և ֆիզիկական:
Մեխանիկական աղտոտումը կապված է քաղաքաշինության, ճանապարհաշինության, ծառահատումների և բնական լանդշաֆտների վրա ազդող այլ միջոցառումների հետ:
Քիմիական աղտոտումը պեստիցիդների, հանքային պարարտանյութերի, թունավոր գազերի, ծանր մետաղների (սնդիկ, կապար, կադմիում և այլն), տարատեսակ աղերի, ճառագայթաակտիվ տարրերի, սինթետիկ լվացամիջոցների ներգործության հետևանք է:
Կենսաբանական աղտոտումն առաջանում է հիվանդածին միկրոօրգանիզմների՝ բակտերիաների, վիրուսների, սնկիկների տարածման միջոցով:
Ֆիզիկական աղտոտումը պայմանավորված է միջավայրի ֆիզիկական հատկությունների՝ լույսի, աղմուկի, ջերմության,խոնավության, ճառագայթման, էլեկտրամագնիսական դաշտիփոփոխություններով:
Մթնոլորտն աղտոտող վտանգավոր նյութերից են ազոտի միացությունները`ազոտի օքսիդը (NO) և ազոտի երկօքսիդը (NO2): Դրանց գլխավոր աղբյուրըբենզինով և դիզելային վառելիքով աշխատող ներքին այրման շարժիչներնեն:
Ազոտի երկօքսիդը դեղին գույնի, բավականին կայուն գազ է և գոյանում էգլխավորապես ավտոմոբիլների արտանետումներից: Այն կարող էմթնոլորտում պահպանվել երեք ժամից ավելի: Հաճախ քաղաքների օդը այդգազից ստանում է շագանակագույն երանգավորում:
Թեմա 1՝ Ենթահարց 2՝ թունավոր նյութերը օդում
1. Պետք է պահպանել մաքուր օդ
2. Ժամանակակից հասարակության մեջ կտրուկ աճում է արտադրական էկոլոգիայի ,դերը իսկ դա կարելի է իրագործել հայտնագործելով ու կատարելագործելով շրջակա միջավայրի պահպանության – ,ինժեներա տեխնիկական միջոցները համաշխարհային մասշտաբով զարգացնելով անթափոն :տեխնոլոգիական արտադրություններ Շրջակա միջավայրի պահպանության գործում կարևոր դեր ունի էկոլոգիական կրթությունն ու դաստիարակությունը
3. ՄԹՆՈԼՈՐՏԸ համարվում է Երկրագնդի արտաքին շերտը և կազմում է Երկրի զանգվածի 1/ ,մլն մասը սակայն նրա դերը :չափազանց մեծ է Չէ ո՞ր մթնոլորտային շերտի առկայությունն է որոշում Երկրի մակերեսի ողջ ջերմային ,ռեժիմը պաշտպանում Երկիրը :տիեզերական ճառագայթումից Սակայն մարդկության արտադրական գործունեությունը ազդում է մթնոլորտի ,վրա որի աղտահարման հիմնական աղբյուրներն են արդյունաբերական ,ձեռնարկությունները ,տրանսպորտը գյուղատնտեսության որոշ (միջոցառումները թունաքիմիկատն ,երի օգտագործում հումքի ),վերամշակում ինչպես նաև ջեռուցման համար օգտագործվող :վառելիքի այրումը և այլն
4. • ՄԹՆՈԼՈՐՏԻ անտրոպոգեն աղտոտման ամենահիմնական :աղբյուրներից մեկը ավտոտրանսպորտն է Ներկայումս ողջ աշխարհում հաշվում է ավելի քան 280 մլն ,ավտոմեքենա որոնք տարեկան մթնոլորտ են արտամղում 50 մլն տոննա ածխաջրածիններ և 200 տոննա :ածխածնի օքսիդներ Բացի այդ շարժիչի աշխատանքի ընթացքում օդի ազոտը միանում `է թթվածնին առաջացնելով ոչ պակաս վտանգավոր ազոտի `օքսիդներ NO և NO2 :և այլն Առանձնապես վտանգավոր է (Il) `ածխածնի օքսիդը CO –ն, որը հայտնի է շմոլ գազ ,անունով որի նույնիսկ 5-10 -մգ ը օդում բացասաբար է ,անդրադառնում մարդու առողջության վրա իսկ 20 -մգ ը :արդեն շնչահեղձ է անում մարդկանց
5. Այն ընկնելով օրգանիզմ 300 անգամ ավելի արագ է , ,միանում հեմոգլոբինի հետ քան թթվածինը ,առաջացնելով կարբօքսիհեմոգլոբին որի պարունակությունը 60%-ից բարձր մահացու է: 0,2 / COմգ լ պարունակող միջավայրում կարելի է գտնվել 1 ,ժամ հետո ի հայտ են գալիս թունավորման ` , ,նշաններ գլխապտույտ սրտխառնոց ոտքերում , ,թուլություն լսողության և տեսողության վատթարացում ,շարժումների կոորդինացիայի խախտում գիտակցության , , ` :կորուստ ցնցումներ շնչառության կանգից մահ
6. ԹՈՒՆԱՎՈՐ ՄԵՏԱՂՆԵՐԻ ԹՈՒՆԱՎՈՐՄԱՆ ԱՍՏԻՃԱՆԸ Նիկել 7746 2-րդ կարգի վնասակար Պղինձ 275 3-րդ կարգի վնասակար Կոբալտ 1730 2-րդ կարգի վնասակար Կապար 22400 1-ին կարգի վնասակար Սնդիկ 31623 1-ին կարգի վնասակար Կադմիում 33124 1-ին կարգի վնասակար 35670Արսեն 1- `ին կարգի վնասակար միացություններըհայտնաբերել են հանքային ջրերում
7. Շմոլ գազը CO-ն , ,անգույն անհոտ թունավոր :գազ է Վատ է `լուծվում ջրում 200 C- 2,3 /100ում գ գ : `1Լավ է լուծվում օրգանական լուծիչներում լ սպիրտում լուծվում է 200սմ3 ,շմոլ գազ իսկ ամոնիակի և ամինների լուծույթները կարելի է օգտագործել :որպես թունավոր խառնուրդներ
8. Թթվային անձրևների առաջացումը պայմանավորված է խոնավ օդում ազոտի և ծծմբի օքսիդների :առկայությանբ (Il) `CO –Ածխածնի օքսիդը ն կարող է առաջանալ ցածր ջերմաստիճաններում վառելանյութերի այրումից թթվածնի պակասի :դեպքում
9. Մթնոլորտային օդի աղտոտման աղբյուր են նաև ,երկաթուղային , -ծովային գետա յին և օդային տրանսպորտի ձևերը: Ծովային տրանսպորտ
10. Երկաթուղային տրանսպորտ
11. Օդային տրանսպորտ
12. Մեծ քանակությամբ ազոտի օքսիդներ են արտանետվում մթնոլորտ ,հրթիռներից ինչն էլ հանդիսանում է օզոնային շերտի քայքայման :պատճառներից մեկը
13. Թունավոր քիմիական միացությունները մեծ քանակությամբ նախատեսված են ռազմական գործողությունների և հակառակորդի :կենդանի ուժը վնասելու համար Թունավոր նյութերը (ԹՆ) օրգանիզմ , ,են թափանցում շնչառական օրգանների մաշկի լորձաթաղանթի և :մարսողական ուղիների միջոցով 50-ից ավելի ԹՆ 1914-1918 -առաջինը կիրառել է Գերմանիան թթ ի առաջին համաշխարային պատերազմի ժամանակ ռազմական .գործողություններում `COClՖոսգենը 2, `HCN , ` ClCN,կապտաթթուն քլորցիանը `S(CHԻպրիտը 2CH2Cl)2, `N(CHեռքլորէթիլամինը 2CH2Cl)3, ` Clքլորպիկրիտը 3CNO2, ` -Cզարինը իզո 3H7OCH3POF, ադամիտը :և այլն
14. 1 – Տնտեսական աղբ 2 – Անասնապահական արգասիքներ 3- Մթնոլորտային խոնավություն 4 – Կոյուղու ջրեր ԱՂՏՈՏՈՒՄԸ ՀՈՂԵՐՈՒՄ ԳՅՈՒՂԱԿԱՆ ՄԻՋԱՎԱՅՐԵՐՈՒՄ
Թեմա 1՝ Ենթահարց 3` Օդի աղտոտման աղբյուրները
- Օդի աղտոտվացությունը Հայաստանում
- Սկսեմ նրանից, որ Հայաստանում շատ են էկոլոգիական խնդիրները: Բայց ընտրեցի օդի ախտոտվածությունը, որովհետև կյանքի համար շատ կարոևր է մաքուր օդը, իսկ երբ մաքուր օդ չկա մենք կարող ենք ամեն տեսակ հիվանդություններով վարակվել` բրոնխիտով, տարբեր ալերգիաներով,դեռմատիտներ (մաշկային հիվանդություններ) նույնիսկ աչքերի հետ կապված խնդիրներ կարող են ի հայտ գալ, օդի աղտոտվածությունից…
- Օդի ախտոտվածությունը կարող է պատճառ դառնալ մաշկային խնդիրների` ալերգիաների: Մարդիկ կարող են փոշուց ալերգիաներ ունենալ,(օրինակ ես`հողից, փոշուց ալերգիա ունեմ): Փոշուց կարող է մարդու մաշկը գռգռվել, և շատ լուրջ խնդիրներ առաջացնել առողջության համար:
- Աչքերը կարող են շատ մեծ վնաս կրել, օդի ախտոտվածության պատճառով: Փոշին լցվելով աչքերի մեջ կարող է առաջացնել մի շարք խնդիրներ:
- Որոշակի հիվանդություննեից հետո, ուզում եմ ներկայացնել շատ հետաքրքիր մի քանի դեպքեր օդի աղտոտվածության պատճառով:
Թեմա 2՝ Ենթահարց 1` Ո՞րն է համարվում մաքուր խմելու ջուր
Մաքուր խմելու ջուրը պիտի պարունակի հանքային աղեր՝ դառը անհամ ջուրը: Եթե ջուրը բաղկացած է 100 մանրէյից, կամ հենց 100 մանրէ պետք չի խմել: Ջրից, եթե քլորի հոտ է գալիս չի կարելի խմել:
Թեմա 2՝ Ենթահարց 2`Ջրի աղտոտման տեսակները
Տարբերում են աղտոտման հետևյալ ձևերը՝
մեխանիկական աղտոտում, որը կապված է քաղաքաշինության, ճանապարհաշինության, ծառահատումների, հողի էրոզիայի հետ,
ֆիզիկական աղտոտում՝ պայմանավորված է միջավայրի ֆիզիկական հատկությունների՝ լույսի, աղմուկի, ջերմության, խոնավության, ճառագայթման, էլեկտրամագնիսական դաշտի փոփոխություններով,
քիմիական աղտոտում՝ պեստիցիդների, հանքային պարարտանյութերի, թունավոր գազերի, ծանր մետաղների (սնդիկ, կապար, կադմիում և այլն), ճառագայթաակտիվ իզոտոպների, ֆտորի միացությունների, սինթետիկ լվացամիջոցների ներգործության հետևանք է,
կենսաբանական աղտոտում, որն առաջանում է հիվանդածին միկրոօրգանիզմների (բակտերիաներ, վիրուսներ, սնկիկներ, կապտականաչ ջրիմուռներ) առկայությունից։
Թեմա 1՝ Հողի աղտոտումը պեստիցիդների, ագրոքիմիկատների և կենսապատրաստուկների վնասակար մնացորդներով.
Օդի և ջրի նման՝ հողը ևս ենթակա է աղտոտման։ Դրա աղտոտման աղբյուրներից մեկը մթնոլորտն է։ Մթնոլորտի աղտոտիչները նստում են հողի մակերևույթին։ Հողի աղտոտման աղբյուրներ են նաև մետաձուլական գործարանների, նավթաարդյունաբերական և արդյունաբերական այլ ձեռնարկությունների թափոնները։ Հողի աղտոտման մեկ այլ աղբյուր է ժամանակակից գյուղատնտեսությունը, որը չի կարող չկիրառել թունաքիմիկատներ և պարարտանյութեր, քանի որ դրանց բացակայության դեպքում բերքի մեծ կորուստներ ունենալու վտանգ է սպառնում։ Վտանգը մեղմացնելու նպատակով շատ տնտեսություններում կիրառվում են վնասատուների դեմ պայքարի կենսաբանական եղանակներ և օրգանական, անվտանգ պարարտանյութեր։
Իսկ հիմա այս թեմաները ընկալելուց հետո անցնենք նախապատրաստական աշխատանքին.
- Մարդկությանը հուզող ինչպիսի՞ էկոլոգիական հիմնախնդիրներ գիտեք
1. Երկրագնդի անտառազրկումը
2. Անապատացումը
3. ջրերի աղտոտվածություն
4. Քաղցրահամ ջրերի որակի վատացումը
- Ո՞րն է էկոլոգիապես մաքուր սնունդը
էկոլոգիապես մաքուր սնունդը մարդու նորմալ կենսագործունեության հիմքն է:
- Ի՞նչ կարծիք ունեք կենսական միջավայրի մասին
Շատ լավ կարծիք ունեմ կենսական միջավայրի մասին, որովհետև օրեցօր ծաղկում է:
- Որո՞նք են առողջ ապրելակերպի սկզբունքները
- Էկոլոգիապես մաքուր սնունդ, մաքուր օդ, մաքուր ջուր
- Առողջ քուն
- Հիգիենա, սպորտ, մարմնամարզություն
- Վատ սովորությունների ձերբազատում
- սթրեսային իրավիճակներից պետք է դուրս գալ հումորով և կատակով:
- Ո՞րն է համարվում մաքուր խմելու ջուր
Մաքուր խմելու ջուրը պիտի պարունակի հանքային աղեր՝ դառը անհամ ջուրը: Եթե ջուրը բաղկացած է 100 մանրէյից, կամ հենց 100 մանրէ պետք չի խմել: Ջրից, եթե քլորի հոտ է գալիս չի կարելի խմել:
- Ջրի շրջապտույտը բնության մեջ
Ջրի շրջապտույտը բնության մեջ: Ջրի ծավալր Երկրի վրա միշտ հաստատուն է և չի փոխվում: Սակայն այդ ջուրը գտնվում է անընդհատ շարժման մեջ՝ անցնելով ջրոլորտի մի բաղադրիչից մյուսին, ինչպես նաև’ մի վիճակից մյուսին: Այսինքն՝ տեղի է ունենում ջրի շրջապտույտ:
Ջուրը, Համաշխարհային օվկիանոսից գոլորշանալով, անցնում է մթնոլորտ, այնտեղից տեղումների ձևով թափվում ցամաքի վրա, որտեղից էլ՝ գետերի ու աղբյուրների միջոցով նորից վերադառնում օվկիանոս:
Տարբերում են ջրի շրջապտույտի երկու տեսակ՝ տեղական կամ փոքր և համաշխարհային կամ մեծ:
Տեղական կամ փոքր շրջապտույտ: Երկրի մակերևույթից Արեգակի ճառագայթների ազդեցության տակ ջուրն արագ գոլորշանում է, և գոլորշիները բարձրանում են վեր: Որոշ բարձրության վրա դրանք, սառելով ու խտանալով, տեղումների ձևով թափվում են Երկրի մակերևույթին: Եթե այս գործրնթացր տեղի է ունենում սահմանափակ տարածքի վրա, ապա կոչվում է տեղական կամ փոքր շրջապտույտ:
Համաշխարհային կամ մեծ շրջապտույտ: Միշտ չէ, որ Երկրի մակերեույթից գոլորշացած ջուրր թափվում է նույն տեղում:
Օվկիանոսից գոլորշացած ջրի մի մասր տեղումների ձեով թափվում է նույն տեղում, իսկ մյուս մասը քամիների ու օդային զանգվածների միջոցով տեղափոխվում է ցամաքի վրա և տեղումների ձևով թափվում այնտեղ: Թափված տեղումների մի մասր սնում է գետերր, կուտակվում լճերի ու ճահիճների մեջ, որոշ քանակություն ներծծվում է երկրակեղևի մեջ՝ առաջացնում ստորերկրյա ջրեր, և վերջապես՝ ցամաքից կարող է նորից գոլորշանալ: Ի վերջո՝ թափված տեղումները, գետերի ու ստորերկրյա ջրերի միջոցով հոսելով, նորից վերադառնում են օվկիանոս: Ջրի այդպիսի շրջապտույտր կոչվում է համաշխարհային կամ մեծ շրջապտույտ:
Ջրի շրջապտույտի նշանակությունը: Ջրի շրջապտույտր չափազանց կարևոր նշանակություն ունի Երկիր մոլորակի համար:
Ջրի շրջապտույտի միջոցով են գոյանում քաղցրահամ ջրի պաշարները ցամաքի վրա: Եթե չլիներ գոլորշացումը, ապա արագ կսպառվեր քաղցրահամ ջուրր, և կյանքր գոյություն չէր ունենա:
Այսպիսով՝ ջրի շրջապտույտի միջոցով անընդհատ թարմանում ու համալրվում են մթնոլորտի և ցամաքի ջրերը: Որքան ջրի շրջապտույտն արագ լինի, այնքան տեղումներ շատ կգոյանան, և գետերի, լճերի ջրերն ավելի արագ կթարմանան:
Միլիոնավոր տարիների րնթացքում ջրի շրջապտույտի միջոցով ցամաքից օվկիանոս են տեղափոխվում հսկայական քանակությամբ տիղմ, ավազ և լուծված նյութեր: Օվկիանոսները հարստանում են ոչ միայն գետերի բերած աղերով, այլև’ տեղում գոլորշացման հետևանքով անջատված աղերով: Դա՝ է պատճառը, որ օվկիանոսի ջուրն աղի է և աստիճանաբար ավելի է աղիանալու:
Վերջապես՝ ջրի շրջապտույտի շնորհիվ է, որ օվկիանոսներում կուտակված ջերմությունը տեղափոխվում է ցամաք՝ մեղմացնելով շրջապատի կլիման:
- Ջրի աղտոտման տեսակները որո՞նք են
Տարբերում են աղտոտման հետևյալ ձևերը՝
մեխանիկական աղտոտում, որը կապված է քաղաքաշինության, ճանապարհաշինության, ծառահատումների, հողի էրոզիայի հետ,
ֆիզիկական աղտոտում՝ պայմանավորված է միջավայրի ֆիզիկական հատկությունների՝ լույսի, աղմուկի, ջերմության, խոնավության, ճառագայթման, էլեկտրամագնիսական դաշտի փոփոխություններով,
քիմիական աղտոտում՝ պեստիցիդների, հանքային պարարտանյութերի, թունավոր գազերի, ծանր մետաղների (սնդիկ, կապար, կադմիում և այլն), ճառագայթաակտիվ իզոտոպների, ֆտորի միացությունների, սինթետիկ լվացամիջոցների ներգործության հետևանք է,
կենսաբանական աղտոտում, որն առաջանում է հիվանդածին միկրոօրգանիզմների (բակտերիաներ, վիրուսներ, սնկիկներ, կապտականաչ ջրիմուռներ) առկայությունից։
- Ի՞նչ է կոշտ ջուրը և ինչպե՞ս են այն վերացնում
Ջրի կոշտությունը պայմանավորված է ջրում պարունակվող կալցիումի, մագնեզիումի, երկաթի, ածխաթթվական և ծծմբաթթվական աղերով: Փափուկ է համարվում այն ջուրը, որի 1 լ-ը պարունակում է մինչև 3 մգ աղեր, կոշտ ջուրը՝ 6-9 մգ։ Մեծ քանակությամբ երկաթի պարունակության դեպքում փոխվում է ջրի գույնը (դառնում է ժանգագույն), զգացվում է մետաղի համը, եռացնելիս կաթսայում գոյանում է գորշ կարմրավուն նստվածք: Կոշտ ջրով սպիտակեղենը լվանալիս մեծանում է օճառի ծախսը և առաջանում է նստվածք, ինչը բացասաբար է անդրադառնում թե՛ կտորի որակի և թե՛ մաշկի առողջական վիճակի վրա։ Կոշտ ջրով լողանալու դեպքում փակվում են մաշկի ծակոտիները, առաջանում է թեփոտում, կորյակներ, ալերգիկ ցան։ Կոշտ ջուր խմելիս օրգանիզմում առաջանում է չլուծվող կալցիումի և մագնեզիումի նստվածք, որը դառնում է միզաքարային հիվանդության պատճառ։ Կոշտ ջրում վատ են եփվում բանջարեղենն ու միսը, իսկ թեյը վատ է թրմվում ևվատանում է համային հատկությունները:
Կենցաղում ջրի կոշտության չափը որոշելու համար տաք ջրի մեջ լուծում են օճառի խոշոր քերվածք, եթե հովանալուց հետո լուծույթը թափանցիկ է մնում, ապա ջուրը փափուկ է։
Ջրի կոշտությունը կարելի է նվազեցնել այն եռացնելով, այդ դեպքում ոչնչանում են նաև մանրէները, հեռանում են լուծված գազերը։ Կենցաղում օգտագործվող ջուրը կարելի է փափկեցնել ինչպես նաև կերակրի սոդայի օգնությամբ։
- Բույսերի պաշտպանություն` բույսերի, բուսական արտադրանքի աճեցման, փորձարկման, պահպանման և փոխադրման վայրերում վնասակար օրգանիզմների դեմ քիմիական և կենսաբանական պայքարի միջոցների օգտագործում.
Բույսերի պաշտպանությունը գյուղատնտեսական արտադրության կարևորագույն օղակներից մեկն է, որն ուղղված է վնասատուներից, հիվանդություններից և մոլախոտերից բերքին հասցվող վնասների չափերի նվազեցմանը, բարձր և որակյալ բերքի ստացմանը: Այս ոլորտի մասնագետի խնդիրն է գյուղատնտեսական մշակաբույսերի վնասատուների, հիվանդությունների հայտնաբերումը և ախտորոշումը, դրանց զարգացման ընթացքում վնասակար փուլերի հանդես գալու ժամկետների ճշտումը, զանգվածային բազմացման և զարգացման պատճառները, դրանց կանխատեսումը և ահազանգումը, վնասատուների և հիվանդությունների տնտեսական վնասակարության ներքին շեմերի որոշումը: Դա հնարավորություն է տալիս մշակելու գիտականորեն հիմնավորված պայքարի միջոցառումների ինտեգրացված համակարգեր, որոնցում կանոնակարգվում է վնասատուների, հիվանդությունների, մոլախոտերի դեմ կիրառվող պայքարի քիմիական միջոցների օգտագործումը:
- Ի՞նչ են ագրոքիմիկատները` պարարտանյութերը, քիմիական հողաբարելավիչները, որոնք նախատեսված են բույսերի սնուցման, հողերի բերրիության բարելավման համար.
Ագրոքիմիկատները նախատեսված են բույսերի սնուցման համար:
Օրգանական պարարտանյութերը բարելավում են հողի ֆիզիկական և քիմիական հատկությունները,կավային հողերը` դառնում են փխրուն, կավաավազային հողերը՝ կապակցված,բարձրանում է հողերում ջրի և օդի թափանցելիությունը, ակտիվանում է մանրէների գործունեությունը, առավել ակտիվ է ընթանում բարդ օրգանական նյութերի քայքայումը,որոնք մշակաբույսերի համար դառնում են մատչելի:
Օրգանական պարարտանյութերից են` գոմաղբը, գոմաղբահեղուկը, տորֆը, թռչնաղբը, կոմպոստները, կանաչ պարարտացումը,բակտերիալպարարտանյութերը, կենսահումուսը և այլն:
- Ի՞նչ է պեստիցիդը` բույսերի պաշտպանության միջոց, ցանկացած նյութ կամ նյութերի խառնուրդ, որը նախատեսված է որոշակի վնասատուների (ներառյալ մարդկանց և կենդանիների հիվանդություններ փոխանցողների, սննդամթերքի, գյուղատնտեսական արտադրանքի, փայտանյութի, կենդանիների կերերի արտադրության, վերամշակման, փոխադրման, իրացման գործընթացներին խանգարող և խոչընդոտող վնասատուների), բույսերի և սնկերի անցանկալի տեսակների կանխարգելման, ոչնչացման կամ պայքարի համար: Պեստիցիդների խմբում ներառված են միջատասպանները (ինսեկտիցիդներ), կրծողների դեմ պայքարի միջոցները (ռոտենդիցիդներ).
Պեստիցիդները թունաքիմիկատաներ են, որոնք օգտագործում են բույսերը վնասատու միջատներից եւ տարբեր հիվանդություններից պաշտպանելու համար։ Երբ մարդն ուտում է պեստիցիդներով մշակված բույսեր, դրանք ընկնում են մարդու օրգանիզմ եւ կուտակվելով կարող են պոտենցիալ բացասական, ընդհուպ մինչեւ քաղցկեղածին ազդեցություն ունենալ:
Մասնագետի խոսքով՝ որոշ պեստիցիդների օգտագործումը, օրինակ՝ ԴԴՏ, ԴԴԵ, դեռեւս տարիներ առաջ արգելվել է, քանի որ դրանք մնում են հողի մեջ եւ աղտոտում են այն, որից հետո արդեն հողից անցնում են բույսերին, կենդանիների մսին եւ մարդու օրգանիզմին։
Պեստիցիդները կարելի է բաժանել մի քանի հիմնական խմբերի
- Հերբիցիդներ, որոնք ոչնչացնում են մոլախոտը
- Ինսեկտիցիդներ, որոնք ոչնչացնում են վնասատու միջատներին
- Ֆունգիցիդներ, որոնք ոչնչքացնում են պաթոգեն սնկերը
- Զոոցիդներ, որոնք ոչնչացնում են վնասակար տաքարյուն կենդանիներին
- Ի՞նչ է սնկասպանները (ֆունգիցիդներ), մոլախոտերի դեմ պայքարի համար նախատեսված նյութերը (հերբիցիդներ), բույսերի աճի կարգավորիչները, ֆերոմոնները, դեֆոլիանտները, դեսիկանտները և ֆումիգանտները.
Տարբերակվում են կոնտակտային և սիստեմային (ներբուսային) ֆունգիցիդներ:
Կոնտակտային ֆունգիցիդները ոչնչացնում են բույսերի տերևայինմակերեսների վրա աճող սնկերի սպորները: Մինչև բույսերի վրասպորների հայտնվելը հարկավոր է նրանցով հավասարաչափ ծածկելտերևային ամբողջ մակերեսը: Եթե սրսկված կոնտակտային ֆունգիցիդինստվածքը ողողվում է անձրևներից, կամ առաջանում է նոր աճեր` տերևներ, ճյուղեր, անհրաժեշտ է լինում սրսկումները կրկնել: Հիվանդածին հարուցիչների դիմացկունությունը այս ֆունգիցիդներինկատմամբ զարգանում է դանդաղ և նրանցից յուրաքանչյուրըբուժման շրջանում կարելի է օգտագործել բազմիցս:
Եթե բույսերի հյուսվածքներն արդեն վարակվել են, ապա կոնտակտ ֆունգիցիդների օգտագործումը դառնում էանօգուտ:
Կոնտակտ ազդեցության ֆունգիցիդները հիմնված են պղնձի աղերի (բորդոյան հեղուկ, պղնձարճարսպ, Կուպրոքսատ, Պղնձի օքսիքլորիդ) ծծմբի (Կոլոիդ ծծումբ, թռչվող ծծումբ, աղացած ծծումբ), տարբերօրգանական միացությունների (Կապտան, Պոլիրամ, Դելան, Էուպարեն) վրա:
Ներբուսային ֆունգիցիդները տարբեր խմբի օրգանական միացություններ են հիվանդածին հարուցիչները, սրանցնկատմամբ ձեռք են բերում դիմացկունություն բավականին արագ: Դրա համար այս խմբի ֆունգիցիդներիցյուրաքանչյուրը տարվա ընթաց քում 2 անգամից ավել չեն օգտագործում: Այս խմբին պատկանողֆունգիցիդներից են` Բայլետոնը, Բենլատը, Սկորը, Ֆունդազոլը, Տոպսին M-ը, Վեկտրան, Իմպակտը, Ռուբիգանը, Սապրորը, Տոպազը, Զատոն, Ստրոբին, Խորուսը:
Այս բոլոր պատրաստուկները ընդունակ են կանգնեցնելու բույսերի հյուսվածքներում սկսված սնկային ինֆեկցիան: Ընդ որում պարտադիր չէ, որ խնամքով, բույսերի ողջ մակերեսը ծածկվի բուժանյութի լուծույթով:
- Որո՞ նք են բույսերի պաշտպանության միջոցները՝ բույսերի վնասակար օրգանիզմների կանխարգելման, դրանց դեմ պայքարի և վերացման համար կիրառվող քիմիական, կենսաբանական միջոցներ:
Բույսերի վնասատուների և հիվանդությունների դեմ պայքարում են ագրոտեխնիկական, կենսաբանական, քիմիական, մեխանիկական և կենսաֆիզիկական եղանակներով։ Էկոլոգիապես անվտանգ է կենսաբանական եղանակը, երբ ստեղծվում են բույսերի հիվանդադիմացկուն սորտեր, իսկ բույսերի կարանտինի միջոցով սահմանափակվում է վնասատուների և հիվանդությունների տարածումը։
1. Ո՞ր շարքում են նյութերը ներկայացված ըստ մարդու օրգանիզմում դրանց
զանգվածային բաժնի նվազման.
1)ածխաջրեր, ջուր, սպիտակուցներ, ճարպեր
2) սպիտակուցներ, ջուր, ճարպեր, ածխաջրեր
3) սպիտակուցներ, ածխաջրեր, ջուր, ճարպեր
4)ջուր, սպիտակուցներ, ճարպեր, ածխաջրեր
2. Սովորականպայմաններում ո՞ր շարքի բոլոր նյութերն են գազեր.
1) կալիումիֆտորիդ, յոդ, ջուր
2) հելիում, սոդա, կավիճ, ազոտ
3) ջրածին, ածխաթթու գազ, թթվածին
4) կարմիրֆոսֆոր, օզոն, բրոմ
3.Ո՞ր քիմիական տարրի ատոմներն են առկա թվարկված բոլոր նյութերի
Բաղադրության մեջ. նատրիումի հիդրօքսիդ,օզոն, ածխածնի (IV) օքսիդ, ջուր,
ազոտական թթու, մագնեզիումի օքսիդ, ջրածնի պերօքսիդ.
1) ջրածին 2) թթվածին 3) քլոր 4) ածխածին
4.Քանի՞ էլեկտրոնէ առկա 8 կարգաթվով տարրի ատոմիվալենտային շերտում.
1) 2 2) 1,806 . 1024 3) 6 4) 8
5. Հետևյալ բանաձևերովո՞ր ջուրն է բնության մեջ առավել տարածված.
1) T217O 2) D216O 3) H216O 4) T218O
6.Որքա՞ն է թթվածին տարրի զանգվածային բաժինը (%) ծանր ջրում` D2O մոլեկուլում.
1) 25 2) 29,4 3) 70,6 4) 80
7.Ջրածնի և թթվածնի 30 լ խառնուրդը պայթեցնելուց հետո մնացել է 3 լ թթվածին:
Որքա՞ն է ջրածնի ծավալային բաժինը (%) ելային խառնուրդում.
8.Երկրագնդի կեղևում թթվածնի և սիլիցիումիզ անգվածային բաժինները հավասար
են 0,48 և 0,28 համապատասխանաբար:
Եկրակեղևում թթվածնի ատոմների թիվը քանի՞անգամ է մեծ սիլիցիումի
ատոմների թվից.
1) 2 2) 2,5 3) 3 4) 4
9.Լաբորատորիայում օզոնստանալունպատակովփականոթումգտնվողթթվածինը
ենթարկել են էլեկտրականպարպման,
ինչպե՞ս է փոխվում անոթում գտնվող գազի զանգվածը.
1) չի փոխվել 2) մեծացել է 1,5 անգամ 3) պակասել է 4) մեծացել է աննշան
10.Օզոնըհայտնաբերումեն այն անցկացնելով կալիումի յոդիդի ջրային լուծույթով, ըստ
հետևյալ ռեակցիայի KI + O3 + H2O = O2 + I2 +KOH Հավասարեցրեք ռեակցիան,
որքա՞ն է ռեակցիայի հավասարման գործակիցների գումարային թիվը.
1) 5 2) 8 3) 3 4) 10
11.Որքա՞ն է ծանր ջրի (D2O) մեկմոլեկուլիզանգվածը (գ).
1) 18 2) 20 3) 2,99. 10-23 4) 3,32. 10-23
12.Փոխազդելենածխածնի 100 ատոմ և թթվածնի 50 մոլեկուլ: Որքա՞ն է ստացված
միացությանմեկմոլեկուլումատոմներիընդհանուրթիվը.
1) 2 2) 4 3) 3 4) 5
13.Համապատասխանեցրե՛քնյութիքիմիականբանաձևը և դրանումդրական և
բացասականօքսիդացմանաստիճանունեցողտարրերիզանգվածայինհարաբերությունը.
Նյութիբանաձև
|
Զանգվածայինհարաբերություն
|
ա) N2O
բ) NO
գ) N2O3
դ) NO2
|
1) 7 : 8
2) 7 : 20
3) 7 : 4
4) 7 : 12
5) 7 : 16
|
Ո՞րշարքիբոլորպատասխաններնենճիշտ.
1) ա3, բ1, գ4, դ3 2) ա3, բ1, գ4, դ5 3) ա2, բ1,գ1, դ5 4) ա2, բ1, գ4, դ5
14. Քանի՞մոլեկուլէ պարունակվում ջրի մեկ լիտրում(ρ=1գ/մլ).
1) 6,02 • 1023 2) 3,35 • 1024 3) 3,34 • 1025 4) 3,35 • 1023
15.Ջրածինը խառնելեն օդին և այրել: Ստացվել է 9 գ ջուր: Ի՞նչ ծավալով (լ)
ջրածին են խառնել օդին.
1) 6,72 2) 11,2 3) 22,4 4) 5,66
16.7,8 գ զանգվածովկալիումըլուծելեն 48,4 գ ջրում:
ա)Գրեքռեակցիայիհավասարումը______________
բ)Որքա՞ն էնյութիզանգվածայինբաժինը (%) ստացվածլուծույթում….
17.ա)Ո՞րզույգնյութերիփոխազդեցությանդեպքումջրածինկանջատվի.
1)խիտ ծծմբական թթու և ցինկ
2).նոսրազոտականթթուևպղինձ
3)խիտաղաթթուևարծաթ
4)նոսրծծմբականթթուևալյումին
բ)Գրեքռեակցիայիհավասարումը______________ Փորձարարական հաշվարկային լաբորատոր աշխատանքներ
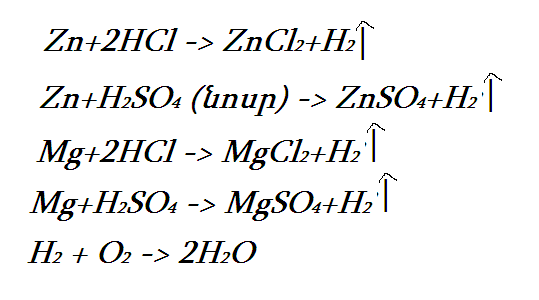
Փորձի համար վերցնում ենք ցինկ (Zn), աղաթթու(HCl) և մագնեզյում (Mg)
Եզրակացություն. Ես եզրակացնում էի, որ այս փորձը կլինի շատ վախենալու, բայց այն շատ հետաքրքիր և ուրախ եղավ: Առաջինը 2,6 գրամ ցինկ կշռեցինք և լցրեցինք փորձանոթի մեջ, այնուհետեվ վրան լցրեցինք աղաթթու, իսկ հետո մագնեզյումի փոքր կտոր, որի արդյունքում պայթյուն տեղի ունեցավ, որը կտեսնեք վիդեոի մեջ:
- Փորձ 1. Ցինկի քլորիդի (կամ սուլֆատի) ստացումը` տեղակալման ռեակցիայի օգնությամբ` ցինկի և աղաթթվի (կամ նոսր ծծմբական թթվի) փոխազդեցությամբ: Գրեք Ձեր կողմից իրականացրած ռեակցիայի հավասարումը և որոշեք ռեակցիայի հետևանքով ստացված աղի զանգվածը (գ), եթե փորձի համար վերցրել եք 2,6 գ մետաղ:
 Փորձի համար վերցնում ենք նատրումի հիդրոքսիդ, ֆենոլֆտալեյն և աղաթթու: Այս փորձը Չեզոքացման ռեակցիյա է
Փորձի համար վերցնում ենք նատրումի հիդրոքսիդ, ֆենոլֆտալեյն և աղաթթու: Այս փորձը Չեզոքացման ռեակցիյա է
Իրականացրեք չեզոքացման ռեակցիա նատրիումի հիդրօքսիդի և աղաթթվի միջև: Գրեք համապատասխան ռեակցիայի հավասարումը և որոշեք ռեակցիայի հետևանքով ստացված աղի զանգվածը (գ), եթե փորձի համար օգտագործել եք նատրիումի հիդրօքսիդի 10 գ 10%-անոց լուծույթ:

Բնապահպանական ստուգատես, 2018
- Մարդկությանը հուզող ինչպիսի՞ էկոլոգիական հիմնախնդիրներ գիտեք
- Ո՞րն է էկոլոգիապես մաքուր սնունդը
- էկոլոգիապես մաքուր արտադրանքը թեև ավելի թանկ է, բայց դրա պահանջարկն այնուամենայնիվ կա
- Ի՞նչ կարծիք ունեք կենսական միջավայրի մասին
- Որո՞նք են առողջ ապրելակերպի սկզբունքները
- Ո՞րն է համարվում մաքուր խմելու ջուր
- Ջրի շրջապտույտը բնության մեջ
- Ջրի աղտոտման տեսակները որո՞նք են
- Ջրի ծավալր Երկրի վրա միշտ հաստատուն է և չի փոխվում: Սակայն այդ ջուրը գտնվում է անընդհատ շարժման մեջ՝ անցնելով ջրոլորտի մի բաղադրիչից մյուսին, ինչպես նաև’ մի վիճակից մյուսին:
- Ի՞նչ է կոշտ ջուրը և ինչպե՞ս են այն վերացնում
Թթուները բաժանվում են 4 խմբի:
- Անթթվածին
- Թթվածնային
- Միահիմք
- Բազմահիմն (երկդիմի, եռահիմն, քառահիմն)
Հայտանյութերի գույնի որոշումը
Բոլոր տեսակի թթուները գունավորում են հայտանյութերը: Լակուսը նյութը դարձնում է կարմիր, մեթիլ օրանժը՝ մուգ վարդագույն, իսկ ֆենոլֆտալեյնը թթուներում չի գունավորում:
Բոլոր տեսակի թթուները գունավորում են հայտանյութերը: Լակուսը նյութը դարձնում է կարմիր, մեթիլ օրանժը՝ մուգ վարդագույն, իսկ ֆենոլֆտալեյնը թթուներում չի գունավորում:
Թթուների ընդահնուր բանաձևն է՝ HnA, ջրաջինը թթուներում +1 օքսիդացման աստիճան ունի:
| Անունները | Բանաձևը | Թթվային մնացորդ |
| Ֆտորաջրածնական թթու կամ պլավիկյան թթու | HF | F– ֆտորիդներ |
| Քլորաջրածնական թթու կամ աղաթթու | HCl | Cl– քլորիդ |
| Բրոմաջրածնական թթու | HBr | Br– բրոմիդ |
| Ծծմբաջրածնական թթու | H2S-երկհիմն | S2- սուլֆիդ |
| Յոդաջրածնական թթու | HI | I– յոդիդ |
| Ազոտական թթու | HNO3 | NO3– նիտրադ |
| Ազոտային թթու | HNO2 | NO2– նիտրիդ |
| Ծծմբային թթու | H2SO3-երկհիմն | SO32- սուլֆիտ |
| Ծծմբական թթու | H2SO4-երկհիմն | SO42- սուլֆատ |
| Ածխաթթու | H2CO3-երկհիմն | CO2- կարբոնատ |
- Անօրգանական շղթաներMe —> հիմնական օքսիդMg+O2— MgO Մագնեզիումի օքսիդMe— Mg+O2— MgO— Mg(OH)2+Cl— MgCl2Փորձ 1MgO ստացումMg+O2— 2MgO+ QԱյրեցինք մագնեզիումը և ստացանք MgO(սպիտակ փոշի)Սպիտակ փոշուց 2,4 գրամ լցրեցինք փորձանօթի մեջ, վրան ավելացրեցինք ջուր և ստացանք հիմք: Մենք ստացել ենք կաթնանաման հեղուկ: Հիմա պետք է համոզվենք, թե մեզ մոտ առաջացել է հիմք, թե ոչ:Փորձ 2Mg(OH)2 ստացումMgO+H2O— Mg(OH)2Համոզվելու համար, որ հիմք է առաջացել օգտագործում ենք հայտանյութ ֆենոլֆտալեինը, որը հիմնային միջավայրում ստանում է մորու գույն:Փորձ 3Mg(OH)2 չեզոքացումՉեզոքացման ռեակցիան փոխանակման ռեակցիա է, որը ընթանում է հիմքի և թթվի միջև, որի հետևանքով առաջանում է աղ և ջուր։Mg(OH)2+ 2HCl— MgCl2+ 2 H2O
Դաս 2. Անօրգանական միացությւոնների հիմնական դասերի վերաբերյալ գիտելիքի ընդհարացում:
1. Անօրգական նյութերի ու դրանց դասակարգումը
Օքսիդների սահմանումը

2 ատոմից կազմված բարդ անօրգանական նյութերը, որնոցից մեկը թթվածինն է -2 օքսիդացման աստիճանով, կոչվում են օքսիդներ:
Քիմիական բանաձևի սահմանումը
Քիմիական բանաձևը նյութի բաղադրության պայմանական գրառումն է քիմիական տարերի նշանների և եթե անհրաժեշտ է ինդեքսենրի (դասիչի) օգնությամբ:
1 ինդեքսը չի գրվում
Օր.` ջուրը կազմված է ջրածնի ու թթվածնի ատոմներից:
Նյութը ունի որակական և քանակական բաղադրություն: Նյութի որակական բաղադրությունը ցույց է տալիս, թե ինչպիսի ատոմներից է նյութը կազմված.
ա) ատոմների թիվը մոլեկուլում,
բ) ատոմների զանգվածային հարաբերությունը բարդ նյութում,
գ) ատոմների զանգվածային բաժինը բարդ նյութում,
դ) ատոմի մոլային բաժինը բարդ նյութում:
- Համար մեկ տարրը Տիեզեքում` Ջրածին: Ջրածնի իզոտոպները`պրոտիում, դեյտերիում, տրիտիում: Համար մեկ նյութը Երկրագնդում `Ջուր: Լուծույթներ: Ծանր ջուր: Ջրածնի պերօքսիդ: Ջրի ֆիզ. քիմ. և ֆիզիոլոգիական հատկությունները: Ջրածինը որպես ապագայի վառելանյութ:

Ջրածին տարրի նշանը
Ջրածնի ատոմն ունի ամենապարզ կառուցվածքը` մեկ դրական լիցքով միջուկի շուրջը սփռված է մեկ էլեկտրոն:

Ջրածնի ատոմի կառուցվածքը
Միացություններ առաջացնելիս ջրածինը հիմնականում ցուցաբերում է մետաղական հատկություն, այսինքն՝ տալիս է մեկ էլեկտրոն և ձեռք է բերում +1 լիցք:
H0−1e→H+
Իսկ որոշ պայմաններում ոչ մետաղական հատկություն` ընդունում է էլեկտրոն (օրինակ՝ մետաղների հետ առաջացած միացություններում) և ձեռք բերում −1 օքսիդացման աստիճան:
H0+1e−→−H−
Միացությունների ձևով ջրածինը չափազանց տարածված տարր է: Նա կազմում է ջրի զանգվածի 11%-ը, մտնում է բոլոր բուսական` մրգերի, բանջարեղենների, թթուների, և կենդանական նյութերի` ճարպերի, սպիտակուցների, ածխաջրերի, նավթի, և շատ այլ հանքային նյութերի բաղադրության մեջ:
Նա կազմում է արեգակի և աստղերից շատերի զանգվածի կեսից ավելին: Արեգակնային համակարգի ամենամեծ մոլորակը` Յուպիտերը, համարյա լրիվ կազմված է ջրածին քիմիական տարրից: Ցածր ջերմաստիճանի և շատ բարձր ճնշման պատճառով ջրածինն այդ մոլորակի վրա գտնվում է պինդ վիճակում:

Ջրածին տարր պարունակող ցանկացած միացություն պարունակում է ջրածնի երկու իզոտոպ` պրոտիում ( 99,98) և դեյտերիում (0,02): Աննշան քանակությամբ հանդիպում է նաև երրորդ իզոտոպը` տրիտիումը:

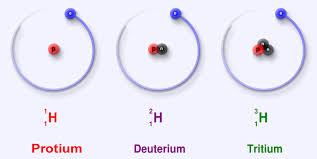
Ջրածնի իզոտոպները
Ջրածին տարրն առաջացնում է ջրածին պարզ նյութը՝
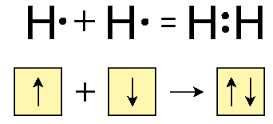
Ջրածնի մոլեկուլի բանաձևն է՝ H2, հարաբերական մոլեկուլային զանգվածը՝ 2,016 (կլորացված 2), մոլային զանգվածը՝ 2 գ/մոլ՝
Ջրածնի մոլեկուլի մոդելը
Ջրածինը բնության մեջ ազատ վիճակում հանդիպում է չնչին քանակով՝ գլխավորապես մթնոլորտի վերին շերտերում: Երբեմն, այն երկրի ընդերքից դուրս է գալիս այլ գազերի հետ հրաբխային ժայթքումների, ինչպես նաև նավթի արդյունահանման ժամանակ:

Ջրածինը վաղուց կարող էր փոխարինել բենզինին
Քաղաքակրթության զարգացումը, ինչպես հայտնի է տեղում չի կանգնած, այլ շարժվում է առաջ: Սակայն վերջին հարյուր տարում, չգիտես ինչու այդ զարգացման ընթացքում չի գտնվել բենզինին փոխարինող այլընտրանքային տարբերակ
Այլընտրանքային վառելիք
Խոսակցությունները էկոլոգիապես ավելի մաքուր և էժան վառելիքի մասին արդեն ընդանում են մի քանի տասնամյակ, բայց այդպես էլ այն շարունակում է մնալ միայն խոսակցություններ:
Օրինակ, ջրածինը բենզինից վատ չի այրվում և բացի այդ նրա այրման ժամանակ ավելի քիչ թունավոր նյութեր են արձակվում: Ինչ վերաբերվում է ջրածնի արդյունահանմանը, ապա նրա ստացման եղանակը լավ հայտնի է, որը ի դեպ լայնորեն օգտագործվում է արդյունաբերության մեջ:
Որպես ջրածնի այլընտրաքային վառելիք չօգտագործման պատճառաբանում, բերվում է այն փաստարկը, որ այն չափազանց պայթունավտանգ է և նման նյութով մեքենայի բաքը լիցքավորելը իրենից մեծ վտանգ է ներկայացնում:
Սակայն, միթե բենզինը պայթունավտանգ չէ? Եվ բացի այդ գոյություն ունի ջրից ջրածին ստանալու էլեկտրոլիզային բավականին լավ հայտնի եղանակ:
Հավանաբար, մի քիչ ցանկության և ֆիանասավորման դեպքում կարելի է պատրաստել ոչ մեծ սարքավորում, որը կարող էր ջրից տարանջատել ջրածինը և մղել ավտոմեքենայի ներքին այրման շարժիչ: Եվ այդ դեպքում պայթունավտանգության հարցը լուծված կլիներ:
1885.-ին Կարլ Բենցի ստեղծած առաջին ներքին այրման շարժիչը
Նշենք միայն, որ առաջին բենզինով աշխատող ներքին այրման շարժիչը ստեղծել է Կարլ Բենցը հեռավոր 1885 թվականին!
Որքան էլ զարմանալի լինի, բայց ամենամեծ շրջանառությունը աշխարհում ընկնում է բենզինին: Օրինակ, ամերիկացիները չնայած բենզինի ցածր գներին, 24 ժամվա ընթացքում ծախսում են նրա վրա 1 միլիարդ դոլար:
Նշենք նաև, որ ռուսաստանի բենզինի և դիզ վառելիքի տարեկան պահանջարկը կազմում է 62 միլիոն տոննա, իսկ 140 միլիոն տոննա էլ արտահանվում է արտասահման:
Ar Արգոնը հայտնաբերել են անգլիացի գիտնականներ Ռամզայը և Ռելեն 1894 թվականին։ Արգոնը իներտ գազերից ամենատարածվածն է։ 40Ar իզոտոպը հանդիպում է կալիում պարունակող միներալներում. այն 40K իզոտոպի ճառագայթաակտիվ քայքայման արդյունք է։ Դրանով է բացատրվում 40Ar-ի բարձր պարունակությունը (ըստ ծավալի` 0,933%) մթնոլորտում։ Արգոնն ստանում են հեղուկ օդի կոտորակային թորմամբ։ Արգոնը կիրառվում է իներտ միջավայր պահանջող քիմիական ու մետաղաձուլական շարժընթացներում՝ հազվագյուտ և գունավոր մետաղների եռակցման, կտրման, հալման ժամանակ։
Իներտ գազեր, քիմիական տարրեր, որոնք կազմում են պարբերական համակարգի 8-րդ խմբի գլխավոր ենթախումբը՝ հելիում՝ He, նեոն՝ Ne, արգոն՝ Ar, կրիպտոն՝ Kr, քսենոն՝ Xe, ռադոն՝ Rn։ Իներտ գազերն այս անվանումն ստացել են իրենց քիմիական մեծ կայունության համար, որի շնորհիվ կոչվում են նաև ազնիվ գազեր։ Այս երևույթը պայմանավորված է նրանց վալենտական թաղանթում էլեկտրոնների ավարտված օկտետի առկայությամբ (բացառությամբ He–ի, որն ունի միայն ավարտված 1s թաղանթ)։ Իներտ գազերի քանակն օդում շատ փոքր է։ Սովորական պայմաններում անհոտ, անգույն, միատոմանի գազեր են։ Էլեկտրական պարպում առաջացնելիս (գովազդային և լուսավորման լամպեր) յուրաքանչյուր գազ գունավորվում է յուրահատուկ գույնով. հելիումը՝ դեղին, նեոնը՝ վառ կարմիր, արգոնը՝ կապույտ, կրիպտոնը՝ կանաչավուն, քսենոնը՝ երկնագույն։
Ջրածինը (H) պարբերական համակարգի առաջին տարրն է։ Առաջին անգամ մաքուր վիճակում ստացել է Հենրի Կավենդիշը 1766 թվականին։ Այն տիեզերքում ամենատարածված տարրն է։ Երկրի վրա այն գտնվում է հիմնականում միացությունների ձևով։ Ջրածինը միացություններում միավալենտ է։
He 1868 թվականին ֆրանսիացի գիտնական Ժանսենը և անգլիացի Լոկիերը արեգակի սպեկտրում հայտնաբերեցին վառ դեղին գիծ։ 1871 թվականին Լոկիերը պարզեց նաև, որ դա բնորոշ է նոր տարրին, և անվանեց հելիում (հունարեն նշանակում է արեգակ)։ 1895 թվականին անգլիացի գիտնական Ռամզայը ճառագայթաակտիվ կլեվիտ հանքաքարի տաքացումից անջատված գազի սպեկտրում նույնպես գտավ նույն դեղին գիծը։ Տիեզերքում, ըստ տարածվածության, հելիումը երկրորդն է ջրածնից հետո, Երկրի վրա 4He իզոտոպն առաջանում է ուրանի, թորիումի և ճառագայթաակտիվ այլ տարրերի տրոհումից։ 4He-ի ատոմի միջուկները (բաղկացած են 2 պրոտոնից և 2 նեյտրոնից) կոչվում են ալֆա-մասնիկներ։
Հելիումն ստանում են օդի խորը սառեցմամբ, որի դեպքում բոլոր գազերը հեղուկանում են, բացի հելիումից։ Նրա սառեցման ջերմաստիճանը հայտնի նյութերի սառեցման ջերմաստիճանից ամենացածրն է՝ -273,15օC։ Հեղուկ հելիումն օգտագործվում է գիտական հետազոտություններում՝ որպես սառեցնող միջոց։ Բարձր ջերմահաղորդականության, քիմիական իներտության շնորհիվ հելիումը կիրառում են ատոմային ռեակտորները սառեցնելու, իսկ ոչ մեծ խտության և անայրելիության շնորհիվ՝ օդապարիկները լցնելու համար։
Նախագիծ 1. Համար մեկ տարրը Տիեզեքում` Ջրածին: Ջրածնի իզոտոպները`պրոտիում, դեյտերիում, տրիտիում: Համար մեկ նյութը Երկրագնդում `Ջուր: Լուծույթներ: Ծանր ջուր: Ջրածնի պերօքսիդ: Ջրի ֆիզ. քիմ. և ֆիզիոլոգիական հատկությունները: Անհատական-հետազոտական աշխատանք՝<<Ջրածինը որպես ապագայի վառելանյութ:>>
 Ջրածինը տիեզերքի ամենատարածված տարրն է։ Ջրածինը թունավոր չէ և օժտված է մեծ ջերմատվությամբ։ Դրա մեկ գրամի այրումից ստացվում է 120 կՋ ջերմություն, մինչդեռ նույն քանակի բենզինից միայն 46 կՋ։ Ընդ որում մթնոլորտն աղտոտող ոչ մի վնասակար նյութ չի առաջանում։ Ջրածինը էկոլոգիապես մաքուր և իդեալական վառելանյութ է։ Այն հեշտությամբ կարելի է տեղափոխել և բաշխել սպառողներին սովորական խողովակաշարով, որոնցով այսօր տեղափոխվում է բնական գազը։ Ջրածինից էլեկտրաէներգիա կարելի է ստանալ ոչ միայն ներկայիս ջերմաէլեկտրակայանում, այլև ավելի մեծ արդյունավետությամբ վերջերս ստեղծված էլեկտրաքիմիական գեներատորներում, այսպես կոչված՝ «վառելիքային սնուցիչներում»: Շատ մասնագետների կարծիքով ջրածնային ներքին այրման շարժիչն ու էլեկտրաքիմիական գեներատորն են պայմանավորելու ավտոմոբիլային փոխադրամիջոցի վաղվա օրը։ Ի՞նչն է, սակայն, խանգարում ջրածնի որպես մաքուր վառելիքի ավելի լայն կիրառությունը։ Գլխավոր խոչընդոտը վառելիքի մյուս տեսակների համեմատությամբ ջրածնի բարձր ինքնարժեքն է։ Այժմ այն հիմնականում ստանում են նավթից, բնական գազից և քարածխից:
Ջրածինը տիեզերքի ամենատարածված տարրն է։ Ջրածինը թունավոր չէ և օժտված է մեծ ջերմատվությամբ։ Դրա մեկ գրամի այրումից ստացվում է 120 կՋ ջերմություն, մինչդեռ նույն քանակի բենզինից միայն 46 կՋ։ Ընդ որում մթնոլորտն աղտոտող ոչ մի վնասակար նյութ չի առաջանում։ Ջրածինը էկոլոգիապես մաքուր և իդեալական վառելանյութ է։ Այն հեշտությամբ կարելի է տեղափոխել և բաշխել սպառողներին սովորական խողովակաշարով, որոնցով այսօր տեղափոխվում է բնական գազը։ Ջրածինից էլեկտրաէներգիա կարելի է ստանալ ոչ միայն ներկայիս ջերմաէլեկտրակայանում, այլև ավելի մեծ արդյունավետությամբ վերջերս ստեղծված էլեկտրաքիմիական գեներատորներում, այսպես կոչված՝ «վառելիքային սնուցիչներում»: Շատ մասնագետների կարծիքով ջրածնային ներքին այրման շարժիչն ու էլեկտրաքիմիական գեներատորն են պայմանավորելու ավտոմոբիլային փոխադրամիջոցի վաղվա օրը։ Ի՞նչն է, սակայն, խանգարում ջրածնի որպես մաքուր վառելիքի ավելի լայն կիրառությունը։ Գլխավոր խոչընդոտը վառելիքի մյուս տեսակների համեմատությամբ ջրածնի բարձր ինքնարժեքն է։ Այժմ այն հիմնականում ստանում են նավթից, բնական գազից և քարածխից:- Տալ օքսիդների խիստ սահմանումը: Ինչով են տարբրվում օքսիդները պերօքսիդներից:
2.
1. Ո՞ր շարքում է գրված միայն ֆիզիկական մարմիններ.
ա) գիրք, մեխ, ալյումին, ազոտ
բ) սեղան, գրիչ, տետր, մատանի
գ) երկաթ, քանոն, ոսկի, թթվածին
դ) պղինձ, ջուր, արծաթ, ջրածին
բ) սեղան, գրիչ, տետր, մատանի
գ) երկաթ, քանոն, ոսկի, թթվածին
դ) պղինձ, ջուր, արծաթ, ջրածին
2. Քանի՞ նյութ է ներկայացված հետևյալ բառակապակցություններում. ջրի կաթիլ, պղնձե թաս, ալյումինե կաթսա, ռետինե գնդակ, պղնձե կուժ, սառցե դղյակ.
ա) 3 բ) 6 գ) 4 դ) 5
3. Նշվածներից ո՞ր շարքում են գրված միայն օրգանական նյութեր.
1) ջուր, թթվածին, կավիճ, սպիրտ
2) կերակրի աղ, սպիտակուց, ճարպ, ազոտ
3) շաքարավազ, քացախաթթու, գլյուկոզ, սպիրտ
4) սոդա, ջուր, ածխաթթու գազ, բենզոլ
1) ջուր, թթվածին, կավիճ, սպիրտ
2) կերակրի աղ, սպիտակուց, ճարպ, ազոտ
3) շաքարավազ, քացախաթթու, գլյուկոզ, սպիրտ
4) սոդա, ջուր, ածխաթթու գազ, բենզոլ
4. Ինչպիսի՞ ագրեգատային վիճակում կարող է գտնվել սնդիկը.
1) միայն պինդ վիճակում
2) միայն գազային վիճակում
3) միայն հեղուկ վիճակում
4) բոլոր երեք վիճակներում
2) միայն գազային վիճակում
3) միայն հեղուկ վիճակում
4) բոլոր երեք վիճակներում
5. Որքա՞ն է ոսկու ձուլակտորի զանգվածը, որի ծավալը 2սմ3 է, իսկ ոսկու խտությունը 19,3 գ/սմ3 է.
1) 38,6գ 2) 9,65գ 3) 3,86գ 4) 1,93գ
1) 38,6գ 2) 9,65գ 3) 3,86գ 4) 1,93գ
6. Համապատասխանեցրեք նյութի հատկությունները և անվանումը.
Հատկությունները
|
Անվանումը
|
ա) բնորոշ հոտով թափանցիկ հեղուկ3)քացախաթթու
բ) ջրում լավ լուծվող պինդ նյութ-2) սախարոզ
գ) մետաղական փայլով պինդ գունավոր նյութ-6) յոդ
դ) ջրում քիչ լուծվող անհոտ, անհամ գազ-4) թթվածին
|
1) կավիճ
5) քլոր
|
7. Ո՞ր շարքում են գրված միայն բարդ նյութերի բանաձևեր.
1) Al, HCl, Cu, Na2SO4 3) H2O, N2, O3, Ni, S8
2) AgBr, H2, CaCO3, P4 4) NaOH, CO2, NH3, CuSO4
8. Ո՞ր տարրական մասնիկներից է կազմված ատոմը.
1) միայն էլեկտրոններից
2) նեյտրոններից և էլեկտրոններից
3) պրոտոններից, էլեկտրոններից և նեյտրոններից
4) միայն պրոտոններից
1) միայն էլեկտրոններից
2) նեյտրոններից և էլեկտրոններից
3) պրոտոններից, էլեկտրոններից և նեյտրոններից
4) միայն պրոտոններից
9. Ո՞ր շարքում է գրված ֆոսֆոր, թթվածին, ածխածին, երկաթ և ազոտ քիմիական տարրերի նշանները.
1) F, C, P, Si, Na
2) O, C, Li, K, Ba
3) P, O, C, Fe, N
4) K, Na, P, Fe, C
1) F, C, P, Si, Na
2) O, C, Li, K, Ba
3) P, O, C, Fe, N
4) K, Na, P, Fe, C
10. Ո՞ր շարքում են առկա միայն կովալենտային կապերով միացություններ.
1) NaCl, HCl, Cl2, NaHCO3 3) H2, NH3, H2O, CH4
2) KBr, HNO3, CaO, P4 4) N2, Br2, CuSO4, Fe
11. Բնութագրեք հետևյալ …. տարրի ատոմը ըստ հետևյալ սխեմայի.
ա) քիմիական տարրի նշանը
Si
բ) կարգաթիվը, միջուկի լիցքը՝ Z- ը
+14
գ) ատոմի բաղադրությունը (պրոտոնների, նեյտրոնների, էլեկտրոնների թիվը)
դ) պարբերության համարը, լրիվ լրացված էներգիական մակարդակների թիվը
ե) խմբի համարը, ենթախումբը (գլխավո՞ր է, թե՞ երկրորդական), արտաքին
էներգիական մակարդակում էլեկտրոնների թիվը
| Պարզ նյութեր | Բարթ նյութեր |
| D2
N2
Fe
Cu
| C12H22O11
NaCl
H2O
D2O
CaSO4
NaHCO3
C3H6O C2H5O4
C2H5OH
CH3COOH
CaCO3
|
Անօրգանական նյութերի հիմնական դասերը
Սահմանում
Օքսիդներենկոչվումերկուտարրիցկազմվածայնբարդանօրգանականնյութերը, որոնցիցմեկըթթվածիննէ -2 օքսիդացման աստիճանով(-2):
Օքսիդների ընդհանուր բանաձևն է
Հիմնային և երկդիմի օքսիդները առաջացնում են մետաղներ, բայց նույն մետաղները չեն: Թթվայինը առաջացնում է ոչ մետաղ:
Դաս 1. Կրկնողություն` Ինչ է նյութը,պարզ և բարդ նյութեր, անօրգանական և օրգանական նյութեր:Մաքուր նյութեր,խառնուրդներ(համասեռ և անհամասեռ):Նյութի բաղադրությունը՝մոլեկուլ,ատոմ , իոն (կառուցվածքը,բաղադրությունը):Նյութի հատկությունները՝ ֆիզիկական, քիմիական, ֆիզիոլոգիական:
Դաս 2- Գործնական աշխատանք 1. Նյութերը դասակարգել,տեղադրել աղյուսակում,անվանել,գրել բանաձևերը: Նկարագրել ֆիզիկական հատկությունները՝ գույնը, ագրեգատային վիճակը(պինդ, հեղուկ, գազային), եռման,հալման ջերմաստիճանները, ջերմա-,էլեկտրահաղորդականությունը, լուծելիությունը ջրում ևայլն:
Բարդ նյութեր Պարզ նյութեր
կերակրի աղ(NaCl) Օ(թթվածին)
շաքար N(ազոտ)
Ջուր (H2O)
Ծանր ջուր (D2O)
Պղնձարջասպ
Խմելու սոդա Նատրիումի հիդրոկարբոնատ
Ացետոն
Մեկ մոլը նյութի այն քանակն է, որը պարունակում է այնքան մասնիկներ որքան ատոմներ, պարունակվում է 12գ. C-ում:
Նյութի զանգվածի պահպանման օրենքը
Քիմիական ռեակցիաների ժամանակ վերցված նյութերի զանգվածը, միշտ հավասար է ստացված նյութերի զանգվածին:
Նյութի բաղադրության հաստատման օրենքը.
Անկախ գտնվելու վայրից և ստացման եղանակներից, նյութերի ունեն հաստատուն բաղադրություն:
Քիմիական հավասարումը քիմիական ռեակցիայի պայմանական գրառումն է, բանաձևերի և գործակիցների միջոցով: Ռեակցիները լինում են 4 տեսակի` միացման, քայքայման, տեղակալման և փոխանակման: Միացման են կոչվում այն ռեակցիաները, որոնց ժամանակ, երկու նյութից ստացվում է մեկ բարդ նյութ (a+b=ab): Քայքայման են կոչվում այն ռեակցիաները, որոնց ժամանակ մեկ բարդ նյութից ստանում ենք մի քանի նյութ (ab=a+b): Տեղակալման ռեակցիաները կատարվում են պարզ և բարդ նյութերի միջև, որտեղ պարզ նյութի ատոմները տեղակլում են բարդ նյութի տարի ատոմների որևէ մեկին(a+bc=ac+b): Փոխանակման ռեակցիաները կատարվում են երկու բարդ նյութերի միջև, որտեղ նրանք փոխանակվում են իրենց բաղադրիչ մասերով (ab+cd=ac+bd):
Պարզ նյութեր
Պարզ նյութերը բաժանվում են մետաղների և ոչ մետաղների: Մետաղները բացի սնդիկից, պինդ են, ունեն փայլ, պլաստիկություն, ջերմա և էլեկտահաղորդականություն: Նրանք վերջին շերտում ունեն 4-ից քիչ էլեկտրոններ: Շերտը ավարտելու համար նրանք կորցնում են էլեկտրոնները, առաջացնելով դրական իոններ: Ոչ մետաղները, եթե պինդ են՝ փխրուն են: Մեծ մասամբ հեղուկ կամ գազային նյութեր են, չունեն փայլ, չունեն ջերմա և էլէկտրահաղորդականություն: Վերջին շերտում ունեն 4-ից շատ էլեկտրոններ և շերտը ավարտելու համար, ձգում են էլեկտրոններ և առաջացնում բացասական իոններ:
Լաբորատոր փորձեր` <<Անօրգանական շղթաներ` մետաղ—> հիմնային-.օքսիդ—>հիմք—>աղ>>, <<ոչմետաղ—> թթվային օքսիդ—> թթու —> աղ: Օքսիդների, ստացումը և քիմիական հատկությունները (հայտանյութերի գույնի փոփոխությունը հիմային, թթվային միջավայրում, թթուների փոխազդեցությունը մետաղների, հիմնային օքսիդների,հիմքերի և աղերի հետ) : 1-բ
2-1
3-3
4-4
5-3
6-4
7-3
8-րդ
9-3
Քիմիական բանաձևը դա նյութի բաղադրության պայմանական գրառումն է, քիմիական նշանների և ինդեքների միջոցով։ Ինդեքսը ցույց է տալիս ատոմների թիվը մոլեկուլում։
Հաշվարկներ ըստ քիմիական բանաձևի
KMNO 4
Կալիումի պեռմանգանաթ(марганцовка)
2.Ինչ տարերից է կազմված նյութը
K-կալիում, MN-մանգան, O-թթվածին
3.Ամեն մի տարրից քանի ատոմ կա մոլեկուլում
1 մոլեկուում կա 1 կալիումի ատոմ, 1 մանգանի ատոմ, 4 թթվածնի ատոմ
4.Հաշվել հարաբերկան մոլեկուլային զանգվածը Mr
Պարոն (KMNO 4 ) = Ar (K) + Ar (MN) + Ar (o) * 4 = 39 + 55 + 16 * 4 = 158
5.Տարրեի զանգվածային հարաբերությունը
m (K): m (MN): m (O) = 39: 55: 64
6. տարրի զանգվածային բաժինը
տարրի զանգվածային բաժինը ցույց է տալիս թե նրա ատոմային զանգվածը, որ մասն է կազմում մոլեկուլային զանվածից։
W (K) = 39 158 * 100% = 25
W (MN) = 55 158 * 100% = 35%
W (O) = 40%
7.նյութը բարդ է թե պարզ
բարդ
NaHCO3-կերակրի սոդա
- Ամեն ինչ ատոմի մասին
- Սովորում ենք թե ինչ է պարբերությունը
- Խումբը և ենթախումբը, ինչ է ցույց տալիս խմբի համարը
- Մենդելևի պարբերական օրենքը
-
Նատրիում
Ատոմի կառուցվածքը Ծծումբ և երկաթ
Մաքուր նյութեր սահմանում
Համասեռ, անհամասեռ խարնուրդներ
Պարզ և բարդ նյութեր
ֆիզիկական և քիմիական երևույթներ
խառնուրդների բաժանման եղանակները
նյութերի հատկությունները
Պարբերական համակարգը
Խառնուրդների բաժանման եղանակները՝ Նշան- Na
1. նյութի փոքրագույն մասնիկն է
Տարրերի առաջին դասակարգը
Ինչ է ցույց տալիս կարգաթիվը
Որոշել հետևյալ տարրերի դիրքը, պարբերական համակարգում և ատոմի բաղադրությունը, համար,8 7,11, 52, 75, 19, 30, 39
2. Հունարենից թարգմանվում է անբաժանելի
Առաջին դասակարգումը հետևյալն է
1. Na, H, C, O
2. Na-1 H-1 C-10-3
3. Պարոն ( NaHCO 3) 23 + 1 + 12 + 16 * 3 = 84
4.
Կարգաթիվը ցույց է տալիս պռոտոնների և էլեկտրոնների թիվը, և միչուկի լիցքը։ Ատոմային զանգվածը կազմված է պռոտոնների, նյետրոնների և էլեկտրոնների զանգվածների գումարից։ Էլեկտրոնների զանգվածը 2000 անգամ
Թթվածին
նշան- O
կարգաթիվ- 8
զանգված- 16
պարբերություն- երկրորդ
խումբը- 6
ենթախումբ- գլխավոր
պռոտոն- 8
նյետռոն- 8
էլեկտրոն- 8
Ազոտ
Նշան-N
կարգաթիվ-7
զանգված 14
պարբերություն- երկրորդ
խումբը- 5
ենթախումբ- գլխավոր
պռոտոն- 7
նյետրոն-7
էլեկտրոն-7
կարգաթիվ-11
զանգվա ծ-23
պարբերություն- 3րդ
խումբը- առաջին
ենթախումբը- գլխավոր
պռոտոն- 11
նյետրոն- 12
էլեկտրոն- 11
Տելուր
նշան- Te1
կարգաթիվ-52
զանգված-128
պարբերություն-5
խումբը-6
ենթախումբը-գլխավոր
պռոտոն- 52
նյետրոն- 76
էլեկտրոն-52
Ռենիում
նշան- Re
կարգաթիվ-75
զանգված-187
պարբերություն-6
խումբը-7
ենթախումբը-երկրորդական
պռոտոն- 75
նյետրոն- 112
էլեկտրոն-75
Նյութի սահմանումը
Այն, ինչից կազմված են բոլոր մարմինները և առարկաները կոչվում է նյութ:Նյութը ունի ծավալ, զանգված և հատկություններ:
Նյութի հատկությունները
1.Ֆիզիկական
Նյութի ֆիզիկական հատկությունները դիտարկում են կամ չափում են առանց նոր նյութ ստանալու:
1.Ֆիզիկական
Նյութի ֆիզիկական հատկությունները դիտարկում են կամ չափում են առանց նոր նյութ ստանալու:
2.Քիմիական
Նյութի քիմիական հատկությունները նյութերի հետ փոխադարձելու ընդունակությունն է:
Նյութի քիմիական հատկությունները նյութերի հետ փոխադարձելու ընդունակությունն է:
3.Ֆիզյոլոգիական
Նյութի ֆիզյոլոգիական հատկությունը նյութերի ազդեցությունը կենդանի օրգանիզմի վրա դրական կամ բացասական:










Комментариев нет:
Отправить комментарий